
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
АМИНОКИСЛОТЫ
|
Читайте также: |
Аминокислоты – органические соединения, содержащие две функциональные группы: карбоксильную –СООН, и аминогруппу –NH2.
Все известные аминокислоты делятся следующим образом:

 Аминокислоты
Аминокислоты
 природные синтетические
природные синтетические
(обнаруженные в растительных (полученные искусственным
 и животных организмах) путем)
и животных организмах) путем)
 |  | ||
заменимые незаменимые протеиногенные
(такие, которые организм (те, которые организм синтезировать (входящие в состав
может синтезировать сам) не может, а должен получать с пищей) белков)
непротеиногенные
(не входящие в состав белков)
Классификация, изомерия
По числу функциональных групп различают:
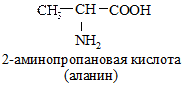 а) моноаминомонокарбоновые
а) моноаминомонокарбоновые
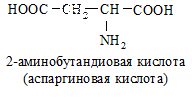 б) моноаминодикарбоновые
б) моноаминодикарбоновые
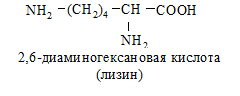 в) диаминомонокарбоновые
в) диаминомонокарбоновые
и др.
В зависимости от расположения аминогруппы по отношению к карбоксильной различают α-, β- и γ-аминокислоты.
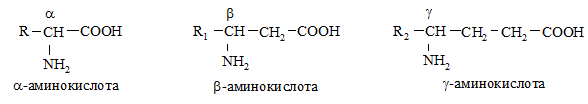
По строению углеводородного радикала аминокислоты классифицируются на алифатические, ароматические и гетероциклические.
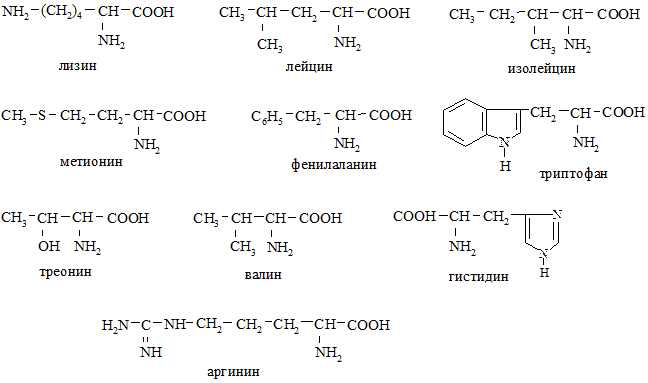
В настоящее время известно более 150 аминокислот, 26 из них входят в состав белков, 10 являются незаменимыми (лизин, лейцин, изолейцин, метионин, фенилаланин, триптофан, треонин, валин, гистедин, аргинин).
Для аминокислот существует 2 вида изомерии: структурная – связана с особенностями строения углеводородного радикала и взаимным расположением функциональных групп и пространственная – оптическая изомерия, связанная с наличием в их молекуле асимметрических атомов углерода (С*).
Практически все природные аминокислоты имеют С* и существуют в виде нескольких оптических изомеров. Например:
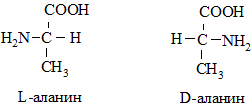
Все протеиногенные аминокислоты относятся к L-ряду, D-формы практически всегда получены синтетическим путем.
СПОСОБЫ ПОЛУЧЕНИЯ
1. Гидролиз белков. Протекает под действием ферментов, кислот или щелочей. Позволяет получить протеиногенные аминокислоты в виде трудноразделяемой смеси.
2. Из галогензамещенных кислот (реакция аммонолиза, аминирования). Проводится при действии водного, спиртового или жидкого аммиака на галогензамещенные карбоновые кислоты.
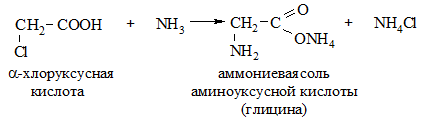
3. Из циангидринов (оксинитрилов). Протекает под действием аммиака на оксинитрилы альдегидов или кетонов с последующим омылением аминонитрила в аминокислоту.
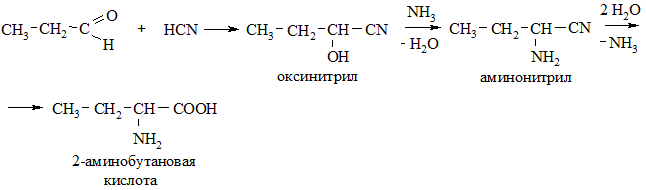
4. Из непредельных кислот – при действии аммиака (реакция протекает против правила Марковникова).
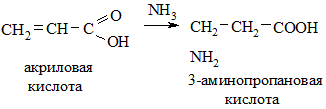
5. Конденсация альдегидов с малоновой кислотой и аммиаком (метод Родионова). Позволяет получить только β-аминокислоты.
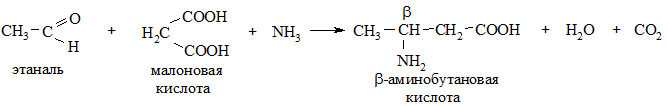
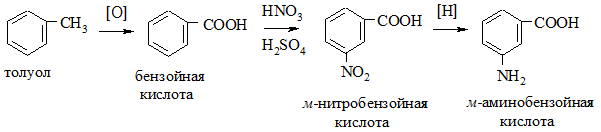
6. Восстановление нитрокислот. В основном используется для получения ароматических аминокислот.
7. Микробиологический синтез – промышленный способ получения аминокислот. Основа метода – микроорганизмы, выращенные на специальной питательной среде, которые продуцируют в процессе жизнедеятельности определенные аминокислоты.
Физические свойства. Особенности строения.
Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде и плохо- в органических растворителях. Не летучи, имеют высокие tплавл. Физические свойства аминокислот обусловлены особенностью их строения. В молекуле аминокислоты аминогруппа, обладающая основными свойствами, вступает во взаимодействие с карбоксильной группой, образуя внутреннюю соль (биполярный ион):
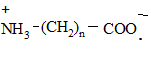
В водных растворах аминокислоты ведут себя как амфотерные соединения. В кислых растворах они проявляют основные свойства, в щелочных – кислотные. Благодаря амфотерности аминокислоты в живом организме играют роль буферных веществ, поддерживающих определенную концентрацию ионов Н+.
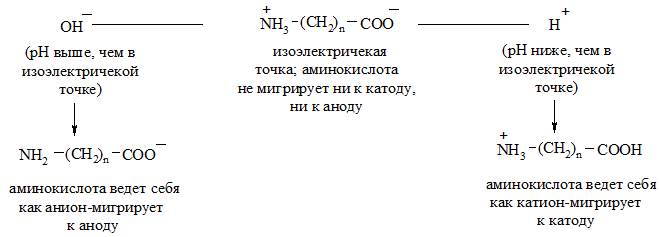
Если через водный раствор аминокислоты пропускать электрический ток, то в зависимости от рН среды аминокислота будет мигрировать либо к катоду, либо к аноду. Значение рН, при котором аминокислота остается электронейтральной и никуда не мигрирует, называется изоэлектрической точкой.
| <== предыдущая страница | | | следующая страница ==> |
| Применение | | | ХИМИЧЕСКИЕ СВОЙСТВА. 1. Образование солей. При взаимодействии с минеральными кислотами и щелочами аминокислоты дают соли |
Дата добавления: 2014-04-15; просмотров: 764; Нарушение авторских прав

Мы поможем в написании ваших работ!