
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
РАСЧЕТ СОСТАВА И КОЛИЧЕСТВА КОЛОШНИКОВОГО ГАЗА И КОЛИЧЕСТВА ДУТЬЯ
2.1Расход природного газа 10,5 м3/100кг чугуна
Состав природного газа, %
| CH4 | C2H6 | C3H8 | N2 | CO2 | S |
| 98,0 | 0,4 | 0,2 | 1,3 | 0,1 | 100,0 |
2.2Анализ летучих веществ кокса, %
| CO2 | CO | CH4 | H2 | N2 | S |
| 29,4 | 34,8 | 0,8 | 4,0 | 31,0 | 100,0 |
2.3В органической массе кокса, % : Н2 = 0,6; N2 = 0,4
Влажность дутья – 13 г/м3 ; содержание О2 в дутье 28%. Степень прямого восстановления rd = 0,3
2.4Расчет баланса углерода
2.4.1Количество углерода в коксе:
С = 100,0 – (9,4+1,5 – 0,08+0,86+0,6+0,4) = 87,32 % ,
где 9,4; 1,5; 0,86; 0,6; 0,4 – содержание в коксе золы, серы, летучих, водорода и азота,
%; 0,08 – содержание серы в золе кокса, %.
2.4.2Вносится коксом углерода:
50,0 × 0,8732 = 43,66 кг
2.4.3Растворяется в чугуне: 4,4 кг
Расходуется на образование метана (0,8 %):
43,66 × 0,008 = 0,35 кг
2.4.4Окисляется шихтой и дутьем:
43,66 – 4,4 – 0,35 = 38,91 кг
2.4.5Расходуется углерода на прямое восстановление:
железа (FeO +C = Fe + CO)
94,28 × 0,3 × (12/56) = 6,06 кг;
кремния (SiO2 + 2C = Si + 2CO)
0,8 (2 × 12/28) = 0,69 кг;
марганца (MnO + C = Mn + CO)
0,5(12/55) = 0,11кг;
фосфора (P2O5 + 5C = 2P + 5CO)
0,05(5 × 12/2 × 31) = 0,05 кг.
где 12, 56, 28, 55, 31 – атомные массы углерода, железа, кремния, марганца, фосфора.
Всего расходуется углерода на прямое восстановление:
6,06 + 0,69 + 0,11 + 0,05 = 6,91 кг
Окисляется углерода у фурм: 38,91 – 6,91 = 32,0 кг.
2.5Расчет количества дутья
2.5.1При сжигании углерода у фурм (2С + О2 = 2СО) требуется кислорода:
32,0(22,4/2 × 12) = 29,87 м3,
где 32 – атомная масса серы.
2.5.2На сжигание углеводородов природного газа в СО потребуется кислорода дутья:
СН4 + 0,5О2 = СО + 2Н2; С2Н2 + О2 = 2СО + 3Н2; С3Н8 + 1,5О2 = 3СО + 4Н2
на 1 м3:
0,5 × 0,98 + 0,004 + 1,5 × 0,002 = 0,5м3,
где 0,98; 0,004; 0,0002 – содержание метана, бутана и пропана в природном газе, дол.ед.
При расходе природного газа 10,5 м3/100кг чугуна потребуется кислорода,м3 :
10,5 × 0,5 = 5,25.
2.5.3Определение кислорода во влажном дутье:
– пересчет влажности дутья в % по объему:
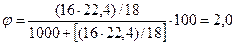 ,
,
тогда кислорода во влажном дутье:
28(1,00-j)+0,5 × j = 28(1,0 – 0,02)+0,5 × 2=28,44%
и количество дутья:
(29,87+5,25)/0,2844 = 123,49 м3,
где 28 – содержание кислорода в дутье, %.
2.6Расчет колошникового газа
2.6.1Количество метана в колошниковом газе:
– образуется метана по реакции С+2Н2 = СН4
0,35(22,4/12) = 0,65 м3;
2.6.2Количество Н2 в колошниковом газе:
– образуется Н2 при разложении природного газа и влаги дутья (количеством СН4 вносимого летучими кокса пренебрегаем, как незначительной величиной)
Н2ПГ = 2 × 0,98 + 3 × 0,004 + 4 × 0,002 = 1,98 м3 в 1 м3 ПГ,
тогда при разложении 10,5 м3 ПГ образуется водорода: 10,5 × 1,98 = 20,79м3
Н2 из влаги дутья, расходуемого на сжигание углерода кокса:
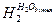 = (29,87/0,2844) × 0,02 = 2,1 м3.
= (29,87/0,2844) × 0,02 = 2,1 м3.
2.6.3Всего образуется водорода:
20,79 + 2,1 = 22,89 м3
2.6.4Из опытных данных известно, что в реакциях косвенного восстановления участвует 1/3 водорода (FeO + H2 = Fe + H2O)
22,89 × 0,33 = 7,55 м3,
– влага восстановления 7,55 × 18/22,4 = 6,07 кг
Тогда количество водорода, переходящего в колошниковый газ: 22,89 – 7,55 = 15,34м3;
– из летучих кокса образуется водорода:
50 × 0,0086 × 0,04 × 22,4/2 = 0,19 м3;
– из органической массы кокса:
50 × 0,006 × 22,4/2 = 3,36 м3;
– расходуется водорода на образование СН4(С+2Н2 = СН4):
0,35 × 22,4 × 2/12 = 1,31 м3
Количество водорода в колошниковом газе:
15,34+0,19+3,36-1,31 = 17,58 м3
2.6.5Количество диоксида углерода в колошниковом газе:
– количество Fe2O3 вносимое шихтой
165,2 × 0,712 = 117,62 кг
– водород в косвенном восстановлении восстанавливает Fe2O3 до FeO, тогда количество Fe2O3, восстанавливающееся водородом составит:
7,55 × 160/22,4 = 53,93 кг
при этом образуется водяного пара:
7,55 × 18/22,4 = 6,07 кг;
– количество Fe2O3, восстанавливаемое СО:
117,62 – 53,93 = 63,69 кг;
– образуется СО2 по реакции : Fe2O3 + CO = 2FeO + CO2
63,69 × 22,4/160 = 8,92 м3;
– количество СО2, образующееся из FeO (FeO + CO = Fe + CO2)
94,23 × 0,7 × 22,4/56 = 26,38 м3,
где 0,7 = 1-0,3 (rd = 0,3); 94,23 – содержание железа в чугуне, %.
– образуется всего СО2 при косвенном восстановлении :
8,92 + 26,38 = 35,30 м3;
– летучие кокса вносят СО2:
50 × 0,0086 × 0,294 × 22,4/44 = 0,06 м3
Всего поступает диоксида в газ:
35,30 + 0,06 = 35,36 м3.
2.7Количество монооксида углерода в колошниковом газе
2.7.1Образуется СО от окисления углерода кокса шихтой и дутьем:
38,91 × 22,4/12 = 72,63 м3,
где 38,91 = 32,0 + 6,91, т.е. количество углерода доходящего до фурм плюс углерод на прямое восстановление, кг.
– при сжигании 1 м3 природного газа
(2СО2 + СО + СН4 + 2С2Н6+ 3С3Н8) = 2 × 0,001 + 0,98 + 2 × 0,004 + +3 × 0,002 = 0,996 м3 ;
– из 10,5 м3 ПГ образуется СО;
10,5 × 0,996 = 10,46 м3;
– остается СО в газе после расхода его части
72,63 + 10,46 – 35,30 = 47,79 м3
2.8Количество N2 в колошниковом газе:
– содержание азота во влажном дутье
72(1,0 – 0,02) = 70,56 %;
– дутье вносит азота
123,49 × 0,7056 = 87,13 м3;
– количество N2 с органической массой кокса
50,0 × 0.004 × 22,4/28 = 0,16 м3;
– с летучими кокса
50,0*0,0086*0,31*22,4/28 = 0,11 м3;
– с природным газом
10,5 × 0,013 = 0,14м3 .
Всего азота в колошниковом газе:
87,13 + 0,16 + 0,11 + 0,14 = 87,54 м3 .
Состав колошникового газа
| Показатель | Составляющие колошникового газа | |||||
| СО2 | СО | СН4 | Н2 | N2 | Σ | |
| Количество, м3 | 35,36 | 47,79 | 0,65 | 17,58 | 87,54 | 188,92 |
| % | 18,7 | 25,3 | 0,3 | 9,3 | 46,4 | 100,0 |
| <== предыдущая страница | | | следующая страница ==> |
| РАСЧЕТ ШИХТЫ, МАТЕРИАЛЬНОГО И ТЕПЛОВОГО БАЛАНСОВ | | | ТЕПЛОВОЙ БАЛАНС |
Дата добавления: 2014-07-23; просмотров: 660; Нарушение авторских прав

Мы поможем в написании ваших работ!