
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ВОЗНИКНОВЕНИЕ ПРОЦЕССОВ ГОРЕНИЯ
В теории горении различают два характерных вида возникновения процессов горения: самовоспламенение и вынужденное (принудительное) зажигание (которое иногда называют просто воспламенением или зажиганием). На практике наиболее часто встречается второй вид возникновения процессов горения.
При рассмотрении условий возникновения реальных процессов горения анализ процессов воспламенения следует проводить на макрокинетическом, т.е. на термодинамическом, уровне, позволяющем установить количественные закономерности, связывающие между собой параметры системы и параметры воспламенения.
Процесс самовоспламенения горючей смеси является наиболее научно разработанным и легко описывается математически. Поэтому с его рассмотрения обычно начинают изучение вопросов возникновения процессов горения [4].
В основе процесса самовоспламенения горючих смесей лежит особенность кинетики химических реакций окисления, которая состоит в неравномерности изменения скорости протекания этих реакций в зависимости от изменения параметров, при которых они реализуются.
5.1. Тепловое самовоспламенение–это реакция окисления горючих веществ, ускоряющаяся и переходящая в реакцию горения. Такой процесс возникновения горения называется самовоспламенением. Самовоспламенение может быть тепловым и цепным. При тепловом самовоспламенении причиной ускорения реакции окисления и возникновения горения является превышение скорости выделения тепла над скоростью теплоотвода, а при цепном - превышение вероятности разветвления цепей над вероятностью их обрыва.
5.2. Температура самовоспламенения
Температура самовоспламенения является показателем пожарной опасности веществ и материалов.
Температура самовоспламенения - самая низкая температура вещества, при которой в условиях специальных испытаний происходит резкое увеличение скорости экзотермических реакций, заканчивающихся пламенным горением.
Значение температуры самовоспламенения применяют при оценке параметров взрывоопасности веществ, при определении группы взрывоопасной смеси для выбора типа взрывозащищенного электрооборудования, при разработке мероприятий по обеспечению пожаровзрывобезопасности технологических процессов.
Температура самовоспламенения не является константой.
Основными факторами, влияющими на tсв являются:
- концентрация горючего в смеси;
- давление;
- объем смеси;
- присутствие катализаторов.
а) Зависимость tсв от концентрации
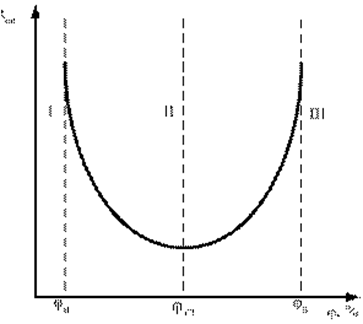
Рис. 5.1. Зависимость температуры самовоспламенения от концентрации горючего в смеси: I - область безопасных концентраций; II - взрывоопасная область; III - пожароопасная область
б) Зависимость tсв от давления
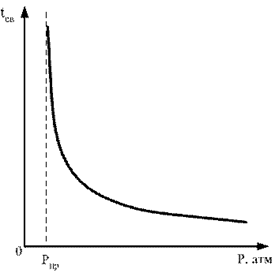
Рис. 5.2. Зависимость температуры самовоспламенения от давления в горючей смеси
в) Зависимость tсв от объема и формы сосуда
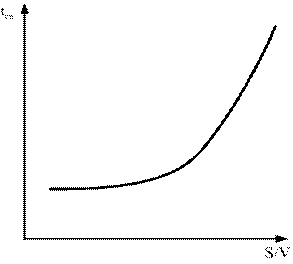
Рис. 5.3. Зависимость температуры самовоспламенения от удельной поверхности сосуда, в котором находится горючая смесь
5.3. Самовозгорание веществ и материалов
Самовозгоранием называют резкое увеличение скорости экзотермических реакций, вызывающих самонагревание веществ, приводящее к возникновению горения при отсутствии источника зажигания.
В зависимости от причины выделения тепла в начальной фазе самонагревания веществ и материалов различают самовозгорание тепловое, микробиологическое и химическое.
Тепловым называется самовозгорание, вызванное самонагреванием, возникшим под воздействием внешнего нагрева вещества выше температуры самонагревания. К тепловому самовозгоранию имеют склонность многие вещества и материалы, к которым можно отнести масла и жиры, каменные угли и т.д.
Самовозгорание масел и жиров часто является причиной пожаров. Существует три вида масел: минеральные, растительные и животные.
Минеральные масла, содержащие предельные углеводороды, к самовозгоранию не способны. Отработанные минеральные масла могут содержать непредельные углеводороды, способные к самовозгоранию.
Растительные (льняное, конопляное, хлопковое и др.) и животные (сливочное) масла по своему составу отличны от минеральных. Они представляют собой смесь глицеридов жирных кислот: пальмитиновой С15Н31СООН, стеариновой С17Н35СООН, олеиновой С17Н33СООН, линолевой С17Н31СООН, линоленовой С17Н29СООН и др. Пальмитиновая и стеариновая кислоты являются предельными, олеиновая, линолевая и линоленовая - непредельными. Глицериды предельных кислот, а следовательно и масла, содержащие их в большом количестве, окисляются при температурах выше 150оС и не способны самовозгораться. Масла, содержащие большое количество глицеридов непредельных кислот, способны к самовозгоранию.
Масла и жиры могут самовозгораться только при определенных условиях:
а) при содержании в масле и жире значительного количества глицеридов непредельных кислот;
б) при большой поверхности окисления масел и жиров и малой теплоотдаче;
в) если жирами и маслами пропитаны какие-либо горючие материалы;
г) при определенной уплотненности промасленного материала.
О количестве глицеридов непредельных кислот в масле и жире судят по йодному числу масла, т.е. по количеству граммов йода, поглощенному 100 г масла. Чем выше йодное число масла, тем в большей степени оно способно к самовозгоранию (льняное масло имеет йодное число в пределах 192-197, конопляное - 145-167, касторовое - 82-86). Если йодное число масел меньше 50, их самовозгорание невозможно.
Масла, жиры или олифы, хранящиеся в бочках, бутылях, резервуаре, самовозгораться не могут, так как площадь поверхности их контакта с воздухом очень мала. Чтобы создать условия самовозгорания, необходимо увеличить поверхность окисления (смочить волокнистые, пористые материалы). Однако для самовозгорания необходимо также, чтобы поверхность окисления была значительно больше поверхности теплоотдачи. Такие условия создаются, когда промасленные материалы сложены в кучи, штабеля, пакеты и прилегают близко один к другому. Способность масел и жиров к самовозгоранию тем больше, чем в большей степени уплотнен промасленный материал. При сильном сжатии материалов вероятность окисления уменьшается за счет ухудшения условий диффузии кислорода к маслу. Способность промасленных материалов к самовозгоранию увеличивается в присутствии катализаторов (солей металлов - марганца, свинца, кобальта).
Наименьшая температура, при которой на практике наблюдали самовозгорание масел и жиров, составляла 10-15°С. Индукционный период самовозгорания промасленных материалов может составлять от нескольких часов до нескольких суток.
Основной причиной самовозгорания углей является их способность окисляться и адсорбировать пары и газы при низких температурах. Рост температуры до 60°С в очаге самовозгорания происходит очень медленно и может быть приостановлен проветриванием штабеля. Начиная с 60°С скорость самонагревания резко увеличивается, поэтому такую температуру угля называют критической. Самовозгоранию углей способствуют их измельчение и присутствие пирита и влаги. Все ископаемые угли по их способности к самовозгоранию делятся на две категории: категория «А» - опасные (к ним относятся бурые и каменные угли), категория «Б» - устойчивые (антрацит и каменные угли марки Т - кузнецкие, донецкие и т.д.).
Для предотвращения самовозгорания углей при хранении:
1.ограничивают высоту штабелей;
2. уплотняют уголь в штабелях с тем, чтобы предотвратить или ограничить проникновение воздуха.
Сульфиды железа FeS, FeS2, Fe2S3 способны также самовозгораться. Основной причиной самовозгорания сульфидов является их способность реагировать с кислородом воздуха при обычной температуре с выделением большого количества тепла:
FeS2 + O2 = FeS + SO2 + 222,3 кДж
При температурах ниже 310°С сульфиды железа в производственной аппаратуре образуются при воздействии сероводорода на продукты коррозии железа.
Самовозгорание сульфидов железа в производственной аппаратуре предотвращают следующими методами:
- защитой от сероводорода из обрабатываемого или хранимого продукта антикоррозийным покрытием внутренней поверхности аппаратуры;
- продуванием аппаратуры паром или продуктами сгорания;
- заполнением аппаратуры водой и медленным спуском ее, что ведет к окислению сульфида без ускорения реакции.
Белый (желтый) фосфор интенсивно окисляется при комнатной температуре. Поэтому он быстро самовозгорается с образованием белого дыма:
4Р + 5О2 = 2Р2О5 + 3100,6 кДж
Хранить и резать фосфор следует под водой, так как на воздухе он может воспламениться от теплоты трения.
К самовозгоранию на воздухе способны также диэтиловый эфир и скипидар. Причина самовозгорания - способность окисляться на воздухе при низких температурах.
Химическим называется самовозгорание, возникшее в результате химического взаимодействия веществ. К группе веществ, которые самовозгораются при контакте с водой, относятся калий, натрий, рубидий, цезий, карбид кальция и карбиды щелочных металлов, гидриды щелочных и щелочноземельных металлов, фосфиды кальция и натрия, негашеная известь, гидросульфид натрия и др.
Щелочные металлы - калий, натрий, рубидий и цезий - взаимодействуют с водой с выделением водорода и значительного количества тепла:
2Na + 2H2O = 2NaOH + H2
Выделяющийся водород самовоспламеняется и горит совместно с металлом только в том случае, если кусок металла по объему больше горошины.
Многие вещества, в основном органические, при смешении или соприкосновении с окислителями способны самовозгораться. К окислителям, вызывающим самовозгорание таких веществ, относятся сжатый кислород, галогены, азотная кислота, перекись натрия и бария, хлорная известь и др.
Например, ацетилен, водород, метан, этилен в смеси с хлором самовозгораются на свету или от света горящего магния.
Нельзя хранить галогены вместе с легковоспламеняющимися жидкостями. При соприкосновении с азотной кислотой самовозгораются скипидар и этиловый спирт.
Микробиологическим называется самовозгорание в результате самонагревания, возникшего под воздействием жизнедеятельности микроорганизмов в массе вещества.
Наибольшей способностью к самовозгоранию обладают фрезерный торф, сено, клевер, силосная масса, листья, солод, хлопок и т.д. Особенно подвержены самовозгоранию недосушенные материалы. Влага и тепло способствуют размножению микроорганизмов. Вследствие плохой теплопроводности растительных материалов выделяющаяся при гниении теплота идет в основном на разогрев материалов, температура повышается и может достичь 70°С. При этой температуре микроорганизмы погибают, но процесс повышения температуры в растительных материалах на этом не заканчивается. Некоторые органические соединения обугливаются уже при 70°С. Образующийся при этом пористый уголь имеет свойство поглощать пары и газы. Адсорбция сопровождается выделением тепла, а в случае малой теплоотдачи уголь нагревается уже до начала процесса окисления. В результате этого температура растительных материалов повышается и достигает 200°С. При 200°С начинает разлагаться клетчатка, входящая в состав растительных материалов, что ведет к обугливанию и дальнейшей интенсификации окисления.
| <== предыдущая страница | | | следующая страница ==> |
| МАТЕРИАЛЬНЫЙ И ТЕПЛОВОЙ БАЛАНС ПРОЦЕССОВ ГОРЕНИЯ | | | ВЫНУЖДЕННОЕ ВОСПЛАМЕНЕНИЕ ГОРЮЧИХ СИСТЕМ |
Дата добавления: 2014-10-14; просмотров: 742; Нарушение авторских прав

Мы поможем в написании ваших работ!