
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ПАРАЛЛЕЛЬНЫЕ РЕАКЦИИ
Иногда исходные вещества реагируют одновременно в нескольких направлениях. Такие реакции называются параллельными.Рассмотрим простейший случай двух параллельных необратимых мономолекулярных реакций
A " B ;
A " C.
Скорость первой реакции
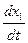 = k1(a – x);
= k1(a – x);
второй
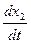 = k2(a – x),
= k2(a – x),
где х1 и х2 — соответственно число молей веществ В и С, образовавшихся к моменту времени t; x = x1+x2—общее число молей вещества А, прореагировавшее к моменту времени t; k1и k2—константы скоростей первой и второй реакций.
Скорость превращения вещества А по двум направлениям будет равна сумме скоростей превращения по каждому из направлений, т. е.
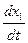 +
+ 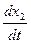 =
= 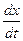 .
.
Далее получим
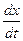 = k1(a – x) + k2(a – x);
= k1(a – x) + k2(a – x);
или
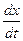 = (k1 + k2)(a – x).
= (k1 + k2)(a – x).
После интегрирования этого уравнения будем иметь
k1 + k2 =  ln
ln 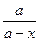 .
.
Это уравнение отличается от аналогичного уравнения для реакции первого порядка тем, что в уравнении стоит сумма констант скоростей обеих параллельных реакций. В случае трех параллельных реакций первого порядка в правой части уравнения будет стоять сумма трех констант.
Уравнение дает возможность определить сумму констант скоростей. Если же нужно найти каждую константу в отдельности, необходимо еще одно уравнение, в которое входили бы эти константы.
Разделив выражения, получим
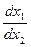 =
= 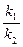 .
.
После интегрирования этого уравнения в пределах соответственно от 0 до х1и от 0 до х2будем иметь
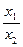 =
= 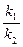 .
.
Определив в некоторый момент времени количества веществ В и С, равные x1и x2, получим отношение констант скоростей обеих параллельных реакций и, следовательно, решив совместно уравнения, получим возможность рассчитать каждую константу в отдельности.
| <== предыдущая страница | | | следующая страница ==> |
| ОБРАТИМАЯ РЕАКЦИЯ ВТОРОГО ПОРЯДКА | | | ПОСЛЕДОВАТЕЛЬНЫЕ РЕАКЦИИ |
Дата добавления: 2014-03-11; просмотров: 356; Нарушение авторских прав

Мы поможем в написании ваших работ!