
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ТЕОРИЯ АКТИВНЫХ СТОЛКНОВЕНИЙ МОЛЕКУЛ
Совокупность стадий, из которых складывается химическая реакция, называется ее механизмом. Молекулярно-кинетическая теория позволяет на основе данных о массе, форме и размерах молекул, энергетической характеристики отдельных связей атомов или атомных групп в молекуле, а также с учетом совокупности энергетических состояний молекулы и внешних условий вычислить скорость процесса. В химической кинетике постулируется, что для осуществления элементарной реакции взаимодействующие молекулы, атомы, радикалы или ионы должны столкнуться. При этом следует учитывать, что молекулы взаимодействуют не только в момент их столкновения в элементарном акте, но проявляется дальнодействие молекул и тогда, когда они не сталкиваются.
В понятие «столкновение» в химической кинетике вкладывается следующий смысл. Молекулы реального газа взаимодействуют друг с другом сложным образом. При малом расстоянии друг от друга они отталкиваются, на большом расстоянии притягиваются. Если диаметр молекулы s, то две одинаковые молекулы придут в соприкосновение тогда, когда расстояние между их центрами станет равным s. Отсюда двигающаяся молекула сталкивается со всеми молекулами, центры которых окажутся на расстоянии s от ее центра. Величина ps2 называется эффективным сечением столкновения. Она равна площади сечения окружающей молекулу воображаемой сферы, в которую не может проникнуть центр другой молекулы. Когда молекулы отталкиваются, то, начиная с некоторого расстояния между ними, путь искривляется и молекулы начнут расходиться.
Когда взаимодействуют молекулы разного диаметра, тогда эффективный диаметр столкновения равен полусумме диаметров сталкивающихся молекул. Применение молекулярно-кинетической теории для расчета скорости химических реакций основано на предположении, что каждое столкновение вызывает элементарный акт взаимодействия. Отсюда следует: скорость химической реакции может быть найдена, исходя из данных о числе столкновений между молекулами. Число столкновений между молекулами Z одного сорта можно подсчитать по формуле
Z = 2n2s2( )1/2 = 2n2s2(
)1/2 = 2n2s2(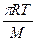 )1/2 ,
)1/2 ,
где n— число молекул в 1 см3; М — молекулярный вес.
Сравнение скорости, рассчитанной по формуле, с найденной опытным путем показало, что последняя значительно меньше. Это говорит о том, что лишь небольшое число столкновений между молекулами приводит к реализации элементарного акта.
Расхождение между числом столкновений и числом реагирующих молекул, а также найденная в опыте зависимость скорости реакции от температуры позволили Аррениусу высказать гипотезу о том, что вступать в реакцию способны только те молекулы, энергия которых превышает некоторую критическую величину Е. Ранее было отмечено, что эта критическая величина есть энергия активации.
Молекулярно-кинетическая теория для числа столкновений молекул, энергия которых превышает некоторую критическую величину Е, дает уравнение
Za = Z0e-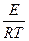 ,
,
где Za — число активных столкновений молекул; Z0 — общее число столкновений в секунду.
Таким образом, реакция возникает только тогда, когда энергия сталкивающихся молекул превышает некоторую критическую величину — энергию активации Е. Ее величину находят из экспериментальной зависимости константы скорости реакции от температуры или по данным о числе активных столкновений.
Для сложных молекул при их активном соударении активные группы должны принимать такую геометрическую конфигурацию, которая обеспечивала бы образование продуктов реакции. В связи с этим в уравнение для скорости реакции вводится стерический множитель Р. Введение его в уравнение указывает на то, что химическая реакция при активном столкновении не абсолютно достоверна, а имеет конечную вероятность, равную Р.
| <== предыдущая страница | | | следующая страница ==> |
| ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА СКОРОСТЬ РЕАКЦИИ | | | ПРИМЕНЕНИЕ ТЕОРИИ СТОЛКНОВЕНИЙ К БИМОЛЕКУЛЯРНЫМ РЕАКЦИЯМ. РАСЧЕТ КОНСТАНТЫ СКОРОСТИ |
Дата добавления: 2014-03-11; просмотров: 625; Нарушение авторских прав

Мы поможем в написании ваших работ!