
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Способы титрования
1. прямое -титрант непосредственно прибавляют к титруемому веществу (один рабочий раствор, пример – титрование щелочи кислотой)
2. обратное –титрование по остатку (два рабочих раствора – основной и вспомогательный, хорошо взаимодействующих друг с другом, например кислота и щелочь или окислитель и восстановитель)
А + В ® Д + Е
В + С ® F + G
метод используют в случае обратимого взаимодействия титранта с определяемым веществом, низкой скорости реакции, отсутствия подходящего индикатора, возможных побочных эффектов.
3. косвенное –титрование заместителя или титрование по замещению
А + Д ® С + Е
С + В ® F + G
метод используют, когда титрант и определяемое вещество не взаимодействуют друг с другом, когда реакция протекает медленно и нестехиометрично.
Расчет результатов титрования
базируется на законе эквивалентов: вещества реагируют между собой в эквивалентных количествах (n1 = n2).
n1 , n2 –число моль экв. титранта и титруемого вещества
n=m/M или n=C×V/1000, [моль]
Формулы для расчетов в титриметрическом анализе.
| Способ расчета | Способ титрования | ||
| прямое | обратное | косвенное | |
| По молярной концентрации раствора |
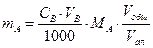
|
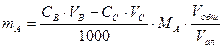
|
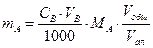
|
| По титру раствора |

|
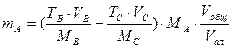
|

|
| По условному титру раствора | 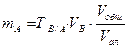
| 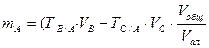
| 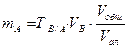
|
mA – масса определяемого вещества, г; МА, МВ, МС – молярные массы веществ А, В, С соответственно (г/моль); CB, TB, VB – молярная концентрация (моль/л), титр (г/мл) и объем (мл) стандартного раствора В; CC, TC, VC – то же для стандартного раствора С; ТВ/А – титр раствора В по веществу А (г/мл); ТС/А – титр раствора С по веществу А (г/мл); Vобщ - общий объем анализируемого раствора, мл; Vал – объем аликвоты.
| <== предыдущая страница | | | следующая страница ==> |
| Титриметрический анализ | | | Расчет рН водных растворов кислот, оснований, солей |
Дата добавления: 2014-04-30; просмотров: 523; Нарушение авторских прав

Мы поможем в написании ваших работ!