
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Химические свойства. Химические свойства алкенов определяются наличием связи С=С
Химические свойства алкенов определяются наличием связи С=С. p-Связь обладает меньшей энергией, чем s-связи, так как энергия С=С связи (611 кДж/моль) меньше удвоенной энергии простой связи (703 кДж/моль). Связь С=С неполярна, но обладает большей поляризуемостью, чем s-связи. Поэтому p-связь легко разрывается под действием как электрофильных ( 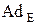 реакции), так и радикальных (
реакции), так и радикальных ( 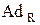 реакции) реагентов. Кроме того, p-связь оказывает влияние на реакционную способность связи С-Н в аллильном положении, что делает возможным протекание реакций радикального замещения атома водорода. Таким образом, молекулы алкенов содержат два основных реакционных центра – связь С=С и связь С-Н в аллильном положении:
реакции) реагентов. Кроме того, p-связь оказывает влияние на реакционную способность связи С-Н в аллильном положении, что делает возможным протекание реакций радикального замещения атома водорода. Таким образом, молекулы алкенов содержат два основных реакционных центра – связь С=С и связь С-Н в аллильном положении:
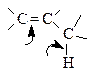
Основные типы реакций алкенов представлены на схеме 7.1.
Схема 7.1. Основные превращения алкенов
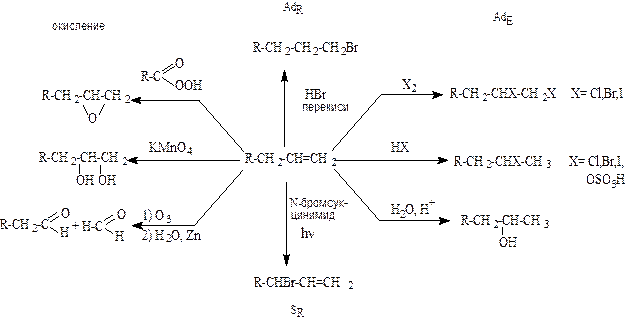
Реакции электрофильного присоединения
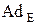 -реакции – основной тип превращений алкенов. По электрофильному механизму к алкенам присоединяются галогены, галогеноводороды, серная кислота, вода и другие электрофильные реагенты. Общий механизм реакции включает ряд последовательных стадий:
-реакции – основной тип превращений алкенов. По электрофильному механизму к алкенам присоединяются галогены, галогеноводороды, серная кислота, вода и другие электрофильные реагенты. Общий механизм реакции включает ряд последовательных стадий:

На первой стадии электрофил образует p-комплекс с алкеном, в котором двойная связь выступает как донор, а электрофил (E-Y или 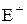 ) как акцептор электронов. Далее p-комплекс медленно перегруппировывается в карбокатион (s-комплекс). На последней стадии происходит быстрое взаимодействие карбокатиона с нуклеофилом (
) как акцептор электронов. Далее p-комплекс медленно перегруппировывается в карбокатион (s-комплекс). На последней стадии происходит быстрое взаимодействие карбокатиона с нуклеофилом ( 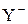 ) с образованием продукта присоединения. Скоростьопределяющей стадией процесса является стадия образования s-комплекса. Следовательно скорость процесса в целом, зависит от стабильности интермедиата – карбокатиона, который близок по энергии к переходному состоянию лимитирующей стадии.
) с образованием продукта присоединения. Скоростьопределяющей стадией процесса является стадия образования s-комплекса. Следовательно скорость процесса в целом, зависит от стабильности интермедиата – карбокатиона, который близок по энергии к переходному состоянию лимитирующей стадии.
Относительная стабильность карбокатионов зависит от возможности делокализации в них положительного заряда. Алкильные группы обладают способностью понижать положительный заряд на соседнем атоме углерода за счет +I-эффекта. Поэтому стабильность карбокатионов возрастает в ряду:

Таким образом, электронодонорные заместители (алкильные группы) увеличивают реакционную способность алкенов, так как, с одной стороны, повышают электронную плотность двойной связи, с другой стороны, стабилизируют карбокатион. Электроноакцепторные заместители действуют в противоположном направлении.
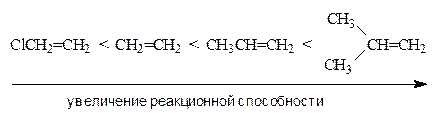
Присоединение галогенов. Галогены легко присоединяются к алкенам с образованием вицинальных дигалогенидов.
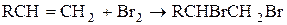
Реакционная способность галогенов возрастает в ряду: 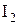 <
< 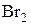 <
< 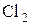 <
< 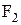
Присоединения брома используют как качественную реакцию на двойную связь. Механизм реакции:
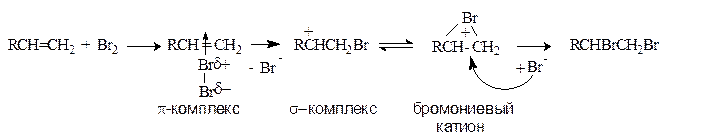
Реакция протекает через образование мостикового бромониевого катиона, существование которого доказано спектральными методами. Образование мостикового иона подтверждается также стереохимическим результатом реакций галогенирования, которые протекают как анти-присоединение, так что результатом присоединения к циклоалкенам является транс-изомер.
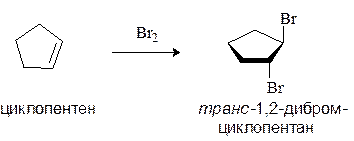
Присоединение протонных кислот. Галогеноводороды, концентрированная серная кислота и вода присоединяются к алкенами с образованием соответственно алкилгалогенидов, алкилсульфатов и спиртов.
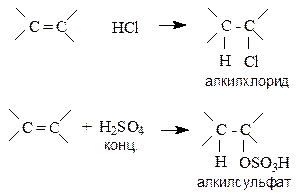
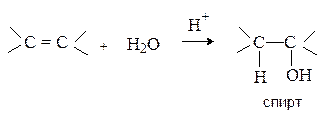
Механизм реакции включает следующие стадии.
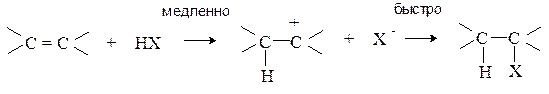
Реакционная способность протонных кислот зависит от их силы. Вода как слабая кислота присоединяется к алкенам в условиях кислотного катализа более сильными протонными кислотами (  ,
, 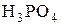 ).
).
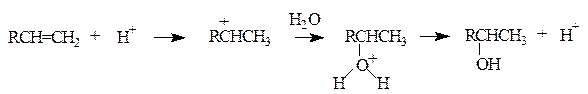
При присоединении протонных кислот к несимметрично замещенным алкенам возможно образование двух разных продуктов. Реакция протекает региоселективно по правилу Марковникова: водород присоединяется к наиболее гидрированному атому углерода.
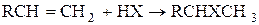
Направление присоединения определяется относительной стабильностью промежуточно образующихся карбокатионов:
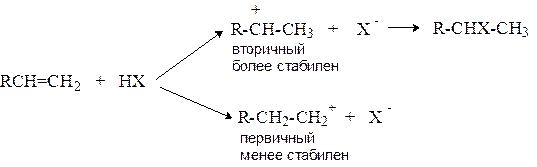
Реакция идет в направлении образования наиболее стабильного вторичного карбокатиона, который образуется с большей скоростью. Энергетическая диаграмма процессов образования первичного и вторичного карбокатионов представлена на рисунке 7.1.
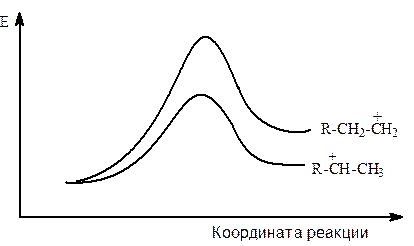
Рис.7.1. Энергетическая диаграмма процесса присоединений протонных кислот к алкенам
Правило Марковникова не является универсальным. Оно может нарушаться в случае изменения механизма реакции, а также при присоединении кислот к алкенам, содержащим электроноакцепторные заместители, обладающие –I-эффектом ( 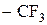 ,
, 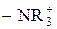 ) или –I- и –М-эффектами (-CHO, -COOH, -CN), например:
) или –I- и –М-эффектами (-CHO, -COOH, -CN), например:
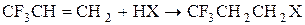
В этом случае реакция протекает в направлении образования наименее дестабилизированного интермедиата, которым является первичный карбокатион, так как в нем электроноакцепторный заместитель не расположен в непосредственной близости от положительно заряженного атома углерода:
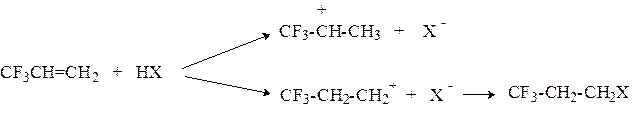
С учетом приведенных фактов можно сформулировать следующее правило:
Электрофильное присоединение несимметричных реагентов к несимметричным алкенам протекает в направлении образования наиболее стабильного карбокатиона.
Это правило позволяет предсказать строение продуктов присоединения к алкенам не только соединений типа HX, но и других несимметричных реагентов (ICl, HOCl).
Присоединение карбокатионов к алкенам. Карбокатионы, которые образуются при присоединении протона к алкенам, являются электрофильными частицами и могут присоединяться к двойной связи другой молекулы алкена, давая продукты алкилирования. Таким образом происходит полимеризация алкенов под действием кислот:
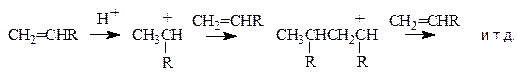
Реакции алкилирования являются способом наращивания углеродной цепи и встречаются в процессах биосинтеза терпенов и стероидов.
| <== предыдущая страница | | | следующая страница ==> |
| НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ | | | Реакции радикального присоединения |
Дата добавления: 2014-05-02; просмотров: 413; Нарушение авторских прав

Мы поможем в написании ваших работ!