
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Средства измерений. Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 210 г
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 210 г;
Бюретка вместимостью 5 см3;
Иономер И–130 М или рН-метр рН–150 М;
Колба мерная вместимостью 100 см3;
Пипетка Мора вместимостью 10 см3;
Электрохимическая ячейка, включающая индикаторный (рН-селективный электрод) и электрод сравнения (хлоридсеребряный).
3 Вспомогательные материалы
Бумага масштабная координатная;
Колбы конические вместимостью 500 см3;
Мешалка магнитная;
Стаканы вместимостью 100 см3;
Холодильник обратный;
Холодильник шариковый.
4 Материалы, реактивы и растворы
Вода дистиллированная;
Кислота серная (H2SO4), раствор – 0,1 моль/дм3;
Натрия гидроксид (NaOH), растворы – 0,05 и 0,1 моль/дм3.
5 Подготовка к выполнению измерений
5.1 Подготовка средств измерений
Иономер и электроды готовят к работе в соответствии с инструкциями по эксплуатации (Приложение Е). рН-метр готовят к работе в соответствии с Приложением Ж.
5.2 Подготовка пробы
В коническую колбу с пришлифованным шариковым холодильником помещают 100 см3 этанола, 100 см3 дистиллированной воды и кипятят в течение 15 мин. Затем смесь охлаждают до комнатной температуры, колбу отсоединяют от холодильника.
6 Порядок выполнения измерений
50 см3 раствора, полученного по п. 6, переносят в стакан, погружают в него электроды и якорь магнитной мешалки. Титруют раствором NaOH (0,1 моль/дм3) до получения скачка и последующего незначительного изменения рН.
К нейтрализованному спирту прибавляют 10 см3 0,1 моль/дм3 раствора гидроксида натрия. Смесь кипятят в конической колбе с обратным холодильником в течение 1 ч, охлаждают до комнатной температуры, закрывая часть холодильника трубкой с натронной известью, затем колбу отсоединяют от холодильника. Содержимое колбы переносят в стакан, добавляют 10 см3 раствора серной кислоты, погружают электроды и якорь магнитной мешалки.
Избыток кислоты оттитровывают 0,05 моль/дм3 раствором NaOH при постоянном перемешивании. Титрант добавляют порциями объемом 0,1 см3 каждая. После каждой порции титранта регистрируют значение рН. Титрование заканчивают зарегистрировав значение рН в трех точках после его резкого изменения.
7 Обработка и вычисление результатов измерений
7.1 Построение кривых потенциометрического титрования и определение КТТ
По данным титрования (п. 6) строят графики в координатах 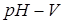 и
и 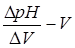 . По графикам находят КТТ и объем раствора NaOH, израсходованный на титрование.
. По графикам находят КТТ и объем раствора NaOH, израсходованный на титрование.
7.2 Расчет массовой концентрации сложных эфиров
Содержание эфиров (q, мг/дм3) в пересчете на уксусноэтиловый эфир в безводном этаноле вычисляют по формуле:
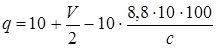 ,
,
где 10 – коэффициент, учитывающий пересчет на 1 дм3 спирта; V – объем 0,05 моль/дм3 раствора NaOH, израсходованный на титрование, см3; 2 – …………..; 10 – ………………;8,8 – масса уксусноэтилового эфира, соответствующая 1 см3 0,1 моль/дм3 раствора гидроксида натрия, мг; 100 – коэффициент, учитывающий пересчет на безводный спирт; c – концентрация этанола, % (об.);
Результаты вычислений округляют до двух значащих цифр после запятой. За окончательный результат измерения принимают среднее арифметическое результатов двух параллельных определений. Окончательный результат округляют до одного знака после запятой.
8 Индивидуальное задание
Определить массовую концентрацию сложных эфиров в пробах спирта и определить его сорт с учетом требований СТБ 1334 [34].
7.7 Лабораторная работа № 7
| <== предыдущая страница | | | следующая страница ==> |
| Определение сложных эфиров в этаноле методом потенциометрии | | | Определение щелочности мучных кондитерских изделий методом потенциометрии |
Дата добавления: 2014-07-19; просмотров: 277; Нарушение авторских прав

Мы поможем в написании ваших работ!