
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Полярность молекул (типы ковалентных молекул)
Следует отличать полярность молекулы от полярности связи. Для двухатомных молекул типа АВ эти понятия совпадают, как это уже показано на примере молекулы HCl. В таких молекулах чем больше разность электроотрицательностей элементов (∆ЭО), тем больше электрический момент диполя. Например, в ряду HF, HCl, HBr, HI он уменьшается в той же последовательности, как и относительная электроотрицательность.
Молекулы могут быть полярными и неполярными в зависимости от характера распределения электронной плотности молекулы. Полярность молекул характеризуется значением электрического момента диполя μм, который равен векторной сумме электрических моментов диполей всех связей и несвязывающих электронных пар в молекулах. Результат сложения зависит от полярности связей, геометрического строения молекулы, наличия неподеленных электронных пар. Большое влияние на полярность молекулы оказывает её симметрия.
Например, молекула СО2 имеет симметричное линейное строение:

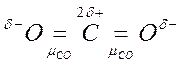 .
.
Поэтому, хотя связи С=О и имеют сильно полярный характер, вследствие взаимной компенсации их электрических моментов диполя молекула СО2 в целом неполярна ( 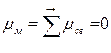 ). По этой же причине неполярны высокосимметричные тетраэдрические молекулы СН4, СF4, октаэдрическая молекула SF6 и т. д.
). По этой же причине неполярны высокосимметричные тетраэдрические молекулы СН4, СF4, октаэдрическая молекула SF6 и т. д.
Напротив, в угловой молекуле Н2О полярные связи О–Н располагаются под углом 104,5º. Поэтому их моменты взаимно не компенсируются и молекула оказывается полярной ( 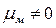 ).
).
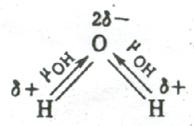
Электрическим моментом диполя обладают также угловая молекула SO2, пирамидальные молекулы NH3, NF3 и т. д. Отсутствие такого момента
свидетельствует о высокосимметричной структуре молекулы, наличие электрического момента диполя – о несимметричности структуры молекулы (табл. 3.2).
Таблица 3.2
Строение и ожидаемая полярность молекул
| Тип | Пространственная конфигурация | Ожидаемая полярность | Примеры |
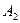
| Линейная | Неполярная | 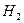 , , 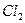 , , 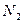
|
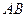
| Линейная | Полярная | 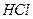 , , 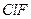
|
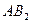
| Линейная | Неполярная | 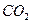 , , 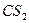 , , 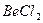
|
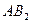
| Угловая | Полярная | 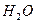 , , 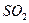 , , 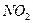
|
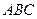
| Линейная | Полярная | 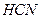
|
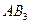
| Плоскотреугольная | Неполярная | 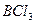 , , 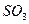
|
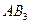
| Тригонально-пирамидальная | Полярная | 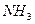 , , 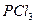 , , 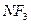
|
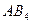
| Тетраэдрическая | Неполярная | 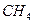 , , 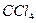 , , 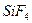
|
На значение электрического момента диполя молекулы сильно влияют несвязывающие электронные пары. Например, молекулы NH3 и NF3 имеют одинаковую тригонально-пирамидальную форму, полярность связей N–H и N–F также примерно одинакова. Однако электрический момент диполя NH3 равен 0,49·10-29 Кл·м, а NF3 всего 0,07·10-29 Кл·м. Это объясняется тем, что в NH3 направление электрического момента диполя связывающей N–H и несвязывающей электронной пары совпадает и при векторном сложении обусловливает большой электрический момент диполя. Наоборот, в NF3 моменты связей N–F и электронной пары направлены в противоположные стороны, поэтому при сложении они частично компенсируются (рис. 3.15).

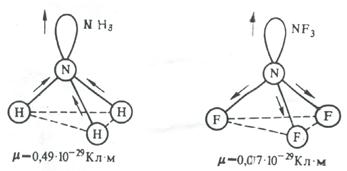
Рис 3.15. Сложение электрических моментов диполя связывающих и несвязывающих электронных пар молекул NH3 и NF3
Неполярную молекулу можно сделать полярной. Для этого её надо поместить в электрическое поле с определенной разностью потенциалов. Под действием электрического поля «центры тяжести» положительных и отрицательных зарядов смещаются и возникает индуцированный или наведенный электрический момент диполя. При снятии поля молекула опять станет неполярной.
Под действием внешнего электрического поля полярная молекула поляризуется, т. е. в ней происходит перераспределение зарядов, и молекула приобретает новое значение электрического момента диполя, становится ещё более полярной. Это может происходить и под влиянием поля, создаваемого приблизившейся полярной молекулой. Способность молекул поляризоваться под действием внешнего электрического поля называют поляризуемостью.
Полярностью и поляризуемостью молекул обусловлено межмолекулярное взаимодействие. С электрическим моментом диполя молекулы связана реакционная способность вещества, его растворимость. Полярные молекулы жидкостей благоприятствуют электролитической диссоциации растворенных в них электролитов.
| <== предыдущая страница | | | следующая страница ==> |
| Полярность и поляризуемость химической связи | | | Ионная связь |
Дата добавления: 2014-09-29; просмотров: 572; Нарушение авторских прав

Мы поможем в написании ваших работ!