
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Кислая среда бесцветная или

 Mn2+ слабо-розовая
Mn2+ слабо-розовая
рн < 7 окраска р-ра
нейтральная среда 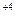
Mn 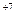 O
O 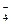
 MnO2 (бурый осадок)
MnO2 (бурый осадок)
рн » 7
щелочная среда +6
 (MnO4)2- (зелёная окраска
(MnO4)2- (зелёная окраска
рн > 7 раствора)
Перманганат–ион окислительные свойства в большей степени проявляет в кислой среде (большее понижение степени окисления).
Обычно для создания в растворе кислой среды используют серную кислоту. Азотную и соляную (хлороводородную) кислоты применяют редко: первая сама является окислителем, вторая способна окисляться. Для создания щелочной среды применяют растворы гидроксида калия или натрия.
Рассмотрим примеры влияния среды на течение реакции с участием пероксида водорода. Пероксид водорода в зависимости от среды восстанавливается согласно схеме:
кислая среда

 H2O2 + 2H+ + 2e- = H2O
H2O2 + 2H+ + 2e- = H2O
pн< 7
 H2O2
H2O2
нейтральная среда
 H2O2 + 2e- = 2OH-
H2O2 + 2e- = 2OH-
щелочная среда
Здесь H2O2 выступает как окислитель. Например:

 2FeSO4 + H2O2 + H2SO2 = Fe2(SO4)3 + 2 H2O
2FeSO4 + H2O2 + H2SO2 = Fe2(SO4)3 + 2 H2O
2 Fe2+ - e- = Fe3+
 1 H2O2 + 2H+ + 2e = 2 H2O
1 H2O2 + 2H+ + 2e = 2 H2O
2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2 H2O
Однако, встречаясь с очень сильным окислителем, таким, как KMnO4, пероксид водорода взаимодействует как восстановитель:
H2O2 - 2e- = O2 + 2H+
Например:
5 H2O2 + 2 KMnO4 + 3H2SO4 = 5 O2 + 2 MnSO4 + K2 SO4 + 8H2O

 5 H2O2 - 2e- = O2 + 2H+
5 H2O2 - 2e- = O2 + 2H+
 2 MnO-4 + 8H+ + 5e = Mn2+ + 4H2O
2 MnO-4 + 8H+ + 5e = Mn2+ + 4H2O
5 H2O2 + 2 MnO-4 + 6H+ = 5 O2 + 2 Mn2+ + 8H2O
Хром в своих соединениях имеет устойчивые степени окисления (+6) и (+3). В первом случае соединения хрома (хромат, дихромат-ионы) проявляют свойства окислителей, во втором - восстановителей. Хромат и дихромат-ионы – сильные окислители, восстанавливаются до соединений Cr3+:
окисленная форма восстановленная форма

 кислая среда
кислая среда

 Cr3+ зеленая окраска
Cr3+ зеленая окраска
рн < 7 раствора
Сr2O72- нейтральная среда

 Сr(OН)3 (серо-голубой осадок)
Сr(OН)3 (серо-голубой осадок)
СrO42- рн » 7
|
|
В щелочной среде ион [Сr(OН)6]3- окисляется до иона СrO42-.
Примеры:
1. Составить молекулярное уравнение для процесса
Na2SO3 + K2Cr2O7 + H2SO4 ®
Решение.
Ионно-молекулярная схема процесса
SO32- + Cr2O72- + 2H+ ® SO42- + Cr3+ + …
в-ль ок-ль продукт продукт
ок-ния в-ния
Уравнения полуреакций и ионно-молекулярное уравнение будут:

 3 SO32- +H2O – 2e- = SO42- + 2H+
3 SO32- +H2O – 2e- = SO42- + 2H+
 1
1
| |
3SO42- + Cr2O72- + 8H+ = 3SO42- + 2Cr3+ + 4H2O
Молекулярное уравнение процесса:
3 Na2SO3 + K2Cr2O7 + 4H2SO4 =3Na2SO4 + Cr2(SO4)3 + K2SO4 + 4H2O.
Пример 2. Составить молекулярное уравнение для процесса
Na3 [Cr(OH)6] + H2O2 + NaOH ®
Решение.
Ионно-молекулярная схема процесса:
[Cr(OH)6]3- + H2O2 + OH 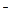 ® CrO42- + H2O + …
® CrO42- + H2O + …
в –ль ок-ль продукт продукт
ок-ия в-ния
Уравнения полуреакций и ионно-молекулярное уравнение будут:

 2 [Cr(OH)6]3- + 2OH
2 [Cr(OH)6]3- + 2OH 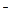 - 3e- = CrO42- + 4H2O
- 3e- = CrO42- + 4H2O
3
| |
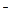

2[Cr(OH)6]3- + 3H2O2 = 2CrO42- + 2OH 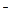 + 8H2O
+ 8H2O
Часто на протекание процесса оказывают влияние концентрация раствора и температура. Так, реакция взаимодействия хлора с разбавленным раствором щелочи при комнатной температуре протекает с образованием гипохлоритов и хлоридов:
CI2 + 2NaOH = NaCIO +NaCI + H2O.
При нагревании до 1000С в присутствии концентрированного раствора щелочи та же реакция протекает с образованием хлоратов и хлоридов:
3CI2 + 6NaOH = NaCIO3 +5NaCI + 3H2O.
На характер протекания реакции может оказывать влияние и катализатор. В присутствии такого катализатора, как иодид-ион I 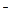 , реакция между Na2S2O3 и Н2О2 протекает по уравнению
, реакция между Na2S2O3 и Н2О2 протекает по уравнению
2Na2S2O3 + Н2О2 =Na2S4O6 + 2NaOH.
В присутствии же другого катализатора – молибденовой кислоты H2MоO4 –та же реакция протекает по уравнению
Na2S2O3 + 4Н2О2 =Na2SO4 + Н2SO4 + 3H2O.
Как следует из рассмотренных примеров, на направление и скорость ОВР влияют многие факторы: природа реагирующих веществ, характер среды, концентрация раствора, температура, присутствие катализатора.
| <== предыдущая страница | | | следующая страница ==> |
| Влияние среды на окислительно-восстановительные реакции | | | Типы окислительно-восстановительных реакций |
Дата добавления: 2014-09-29; просмотров: 402; Нарушение авторских прав

Мы поможем в написании ваших работ!