
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Введение 7 страница
|
Читайте также: |
Способность продуцировать, органические кислоты при росте на средах с углеводами широко распространена среди мицелиальных грибов родов Aspergillus, Rhizopus,Candida и другие грибы. Грибы обнаруживаются в виде плесневого налета, состоящего из вегетативного мицелия, несущего конидиеносцы с конидиями. На поверхностях питательных сред пенициллы и аспергиллы образуют плоские колонии, состоящие из вегетативного мицелия. На определенной стадии развития грибов образуются воздушные гифы, на которых развиваются конидиеносцы несущие конидии, которые служат для размножения плесневых грибов.
Получение лимонной кислоты
В 1891 г. Немецкий ученый Вемер установил способность плесневых грибов продуцировать органические кислоты. При выращивании Aspergillus niger на среде с сахаром им было констатировано выделение щавелевой кислоты. Через два года Вемер обнаружил лимонную кислоту, накапливающуюся в среде при выращивании грибов, названных им Citromyces (C. pfefferianus C. glaber). Впоследствии Citromyces были отнесены к роду Penicillium. Вемер пытался осуществить производство лимонной кислоты с помощью грибов из сахара. Работа окончилась неудачей в связи с рядом трудностей, непреодолимых в то время. В 1917 г. американский ученый Кэрри сообщил о способности ряда штаммов Aspergillus niger продуцировать лимонную кислоту наряду с щавелевой. Это было важное открытие, поскольку в отличие от плохо растущих пенициллов, Aspergillus niger характеризовался мощным и быстрым ростом. Штамм гриба, с которым работал Кэрри, и условия ведения процесса были в дальнейшем использованы в микробиологических процессах производства лимонной кислоты. Способность образовывать лимонную кислоту при росте на средах с углеводами – свойство, широко распространенное среди мицелиальных грибов. До недавнего времени в производстве использовали специально селекционированные штаммы гриба, выделенные из природных источников. Последние два десятилетия в качестве продуцентов все шире применяются экспериментально полученные мутантные штаммы, отличающиеся от природных рядом положительных свойств, в первую очередь более высоким выходом целевого продукта. Для получения лимонной кислоты в лабораторном и промышленном масштабе, кроме грибов рода Aspergillus (в том числе виды A. awamori, A. clavatus, A. fumaricas, A. japonicus, A. wentii), используются грибырода Penicillium (в том числе P. chrysogenum, P. citrinum, P. citrogenium, P. luteum), а также Botrytis cinerea, Paecilomyces divaricatum, Mucor piriformis, Poliporus anceps и некоторые другие грибы. Объем мирового производства цитрата составляет 400 тыс. т/год. Самый крупный производитель лимонной кислоты - США. Производство лимонной кислоты принадлежит к числу старейших промышленных микробиологических процессов: оно было организовано в 1893 г. С этого момента параллельно развитию фундаментальной микробиологии велись изыскания оптимальных продуцентов и технологических вариантов процесса ферментации.Способность различных грибов, продуцировать лимонную кислоту проявляется в строго определенных условиях культивирования. Культуры грибов при избытке питательных веществ не накапливают лимонной кислоты, а образуют значительную биомассу и окисляют сахар до CO2 и H2 O. Синтез лимонной кислоты грибом-продуцентом осуществляется обычно на средах с высокой концентрацией углевода (5-20%). Наилучшим субстратом для продуцентов является – сахароза.Накопления кислоты имеет место при ограничении роста гриба одним из минеральных компонентов среды (F, Mn, P, N) или несколькими компонентами одновременно. Преимущественное образование лимонной кислоты происходит при культивировании продуцента при низким значении рН среды. В таких условиях синтез других органических кислот подавляется. Процесс кислотообразования осуществляется в условиях культуры молекулярным кислородом.
В процессе ферментации микробиологического производства, можно выделить две фазы: 1) активного роста гриба и 2) интенсивного кислотообразования, рост мицелия в этот период становится незначительным.При производстве лимонной кислоты применяются три способа ферментации:
1. Культивирование продуцента на поверхности твердой питательной среды (твердофазная ферментация).
2. Поверхностное культивирование на жидкой среде.
3. Погруженное глубинное культивирование.
Культивирование на поверхности твердой среды. Гриб-продуцент выращивают в неглубоких лотках на поверхности влажных отрубей риса или пшеницы. Во время ферментации рН массы отрубей падает до 1,8-2,0. после окончания процесса лимонная кислота вместе с небольшим количеством одновременно образовавшихся глюконовой и щавелевой кислот экстрагируется водой, а затем осаждается в виде соли кальция. В связи с тем, что отруби богаты железом и другими микроэлементами используют штаммы Aspergillus niger, не чувствительные к высоким концентрациям металлов. Поверхностное культивирование на жидкой среде. Поверхность жидкой среды, разлитой в неглубокие кюветы, засевают конидиями гриба – продуцента. Кюветы размещают на стеллажах в термостатированных «бродильных камерах». Гриб развивается в виде плотной пленки на поверхности питательной среды, содержащей высокие концентрации сахара. Образующаяся лимонная кислота переходит из клеток мицелия в раствор, из которого после окончания процесса ее осаждают в виде кальциевой соли, а затем переводят в форму свободной кислоты и кристаллизуют.
Глубинное культивирование. Производство лимонной кислоты методом глубинного культивирования обладает многими преимуществами по сравнению другими методами культивирования. Применение глубинного метода позволяет повысить эффективность использования производственных площадей, увеличить масштабы производства, механизировать трудоемкие работы и почти полностью автоматизировать технологический процесс получения кислоты. При этом методе применяют специально селекционированные природные штаммы или мутанты. Штамм сохраняется в виде конидий, отделенных от мицелия. В качестве посевного материала для ферментации используются конидия гриба, смешанные с активированным углем или тальком. Процесс ферментации включает два этапа: 1) выращивание мицелия в посевном аппарате; 2) рост мицелия и кислообразование в основном ферментаторе. В предварительно простерилизованной посевной аппарат загружают питательную среду, для подращивания посевного материала, содержащую 3-4% сахара, затем через инокулятор вносят суспензию спор гриба. Сразу после засева в ферментер подают стерильный воздух и включают мешалку. Прорастание спор и формирование мицелии гриба происходит при непрерывном продувании воздуха через культуральную жидкость и перемешивании ее. Температура среды поддерживает около 32о С. Через 20-36 ч мицелии гриба вместе с культуральной жидкостью передается в основной ферментатор. Основной процесс в производственном ферментаторе продолжается 5-7 суток. В конце ферментации концентрация лимонной кислоты достигает 50-120% (в зависимости от качества сырья и активности штамма) и составляет 80-95% общей суммы кислот. Когда активность кислотообразования падает, процесс прекращают. Культуральный раствор отделяют от мицелия путем фильтрацией или другим способом и передают в химический цех для выделения и последующей кристаллизации лимонной кислоты ( Рис. 1).




Рис. 1. Технологическая схема получения лимонной кислоты глубинным способом культивирования (Карклиньш и Пробок, 1972):
 1 – бак с мелассой; 2 – приемный бак; 3 – весы; 4 – выварочный котел; 5 - центробежный насос; 6 – промежуточная емкость; 7 – стерильная колонка; 8 – выдерживатель; 9 – холодильник; 10 – посевной ферментатор; 11 - производственный ферментатор; 12 – противобактериальные фильтры; 13 – емкость для хранения мелассы; 14 – промежуточный сборник; 15 – барабанный вакуум-фильтр; 16 – корыто для приема мицелия; 17 - вакуум-сборник для мицелия; 18 – вакуум-сборник фильтрованного (сброженного) раствора.
1 – бак с мелассой; 2 – приемный бак; 3 – весы; 4 – выварочный котел; 5 - центробежный насос; 6 – промежуточная емкость; 7 – стерильная колонка; 8 – выдерживатель; 9 – холодильник; 10 – посевной ферментатор; 11 - производственный ферментатор; 12 – противобактериальные фильтры; 13 – емкость для хранения мелассы; 14 – промежуточный сборник; 15 – барабанный вакуум-фильтр; 16 – корыто для приема мицелия; 17 - вакуум-сборник для мицелия; 18 – вакуум-сборник фильтрованного (сброженного) раствора.
Производство уксусной кислоты
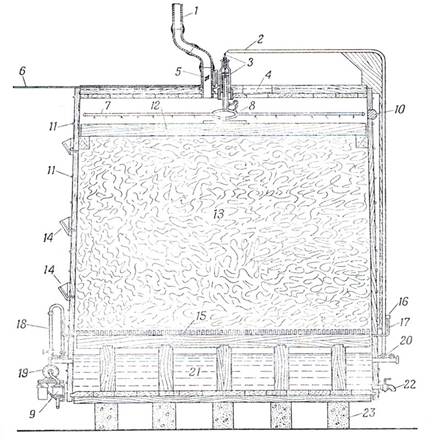
Уксусная кислота (СН3СООН) – имеет наиболее важное значение среди всех органических кислот. Она широко используется в пищевой, химической, микробиологической промышленности, в медицине. Ежегодно в мире производят более 100 тыс. т уксусной кислоты. Уксус применяют в пищевой промышленности. Его используют при выработке многих химических веществ, включая каучук, пластмассы, волокна, инсектициды. Получение уксусной кислоты из спиртосодержащих жидкостей было известно более 10 тыс. лет назад. В те времена древние греки и римляне использовали уксус в качестве освежающего напитка и получали, главным образом, оставляя вино открытым. В больших масштабах уксус долго получали в плоских открытых бочках, в которых пленка бактерий плавала на поверхности. В XIX веке поверхностные процессы стали заменять более эффективными. Так, был разработан процесс в струйном генераторе. В середине ХХ века появились глубинные процессы ферментации. Усовершенствованный генератор Фрингса (рис. 2.) используется в настоящее время.



 |
Рис.2. Схема получения уксусной кислоты. Поперечный разрез
генератора Фрингса.
1-выводная труба; 2-каучуковая трубка; 3-стеклянный механизм, регулирующий ток жидкости; 4-смотровое отверстие, закрытое стеклом; 5-регулятор тяги; 6-стеклянная трубка диаметром 1см, идущая к газовому счетчику; 7-боковые лучи распылителя диаметром около 2,2см; 8 – распылитель; 9-фильтр для уксуса; 10-втулка, закрывающая отверстие для работы распылителя; 11-обручи толщиной 2,5см; 12-Упор для распылителя диаметром 15,2-20,3см; 13-Стружки; 14-Термометры для измерения температуры внутри генератора; 15-Деревянная решетка с отверстиями 3,7-7,5см; 16-Фильтр для воздуха; 17-Труба для поступления воздуха (по 10 в каждом генераторе); 18-Счетчик циркулирующей жидкости; 9-Центробежный насос; 20-Змеевик холодильника диаметром 2,5см из нержавеющей стали, лежащий внутри медной трубки диаметром 3,75см, в которой циркулирует холодная вода; 21-Сточная камера; 22-Кран для слива готового уксуса; 23 – Цементные блоки.
Процессы получения в генераторе Фрингса, один из быстрых способов производства уксуса. Генератор состоит из герметического биореактора диаметром обычно около 4,25 м и высотой 4,5 м, снабженного вспомогательными механизмами. Генератор устанавливают на бетонных брусьях, для того чтобы воздух мог свободно циркулировать под аппаратом. Внутри биореактора, на небольшом расстоянии от его дна, находится деревянная решетка, на которую помещают буковые стружки. Генератор наполняют стружками, оставляя наверху свободное пространство около 40 см высотой. Между деревянной решеткой и дном генератора находится камера для сбора готовой продукции. В самом низу этой камеры имеется кран или втулка для удаления готового уксуса. На небольшом расстоянии от дна генератора расположен змеевик для охлаждения. Прошедший через стружки подкисленный спиртовой раствор попадает в нижнюю камеру, а оттуда накачивается в трубу, сделанную из нержавеющей стали или какого-либо другого кислотоустойчивого материала, где раствор охлаждается. Для охлаждения стальная труба заключена в другую трубу из меди, несколько большего диаметра, в которой циркулирует холодная вода. Затем частично сброженное сусло при помощи специального насоса из нержавеющей стали снова поднимается по резиновой трубке из холодильника в верхнюю часть биореактора. Здесь жидкость, проходя через специальный стеклянный аппарат, попадает в распылитель из нержавеющей стали. Количество проходящего через генератор кислорода зависит от регулятора тяги, расположенного в выходном отверстии диаметром около 10 см – оно находится на самом верху генератора. Это отверстие служит для выхода воздуха. Воздух поступает в генератор через несколько (обычно 10) специальных клапанов, расположенных по окружности биореактора на уровне нижней деревянной решетки. Эти клапаны снабжены приспособлениями для фильтрации воздуха. Для определения температуры брожения в различных отделах биореактора имеются термометры. Генератор снабжен двумя счетчиками: первый, расположенный около насоса, служит для измерения скорости циркуляции сусла, второй — для определения скорости тока воды в холодильнике. Сусло пропускают несколько раз через буковые стружки до получения уксуса желаемой крепости. Питательная жидкость, содержащая спирт и кислоту, проходя через холодильник, охлаждается до желаемой температуры, что позволяет точно контролировать температуру внутри биореактора. Охлажденная смесь вновь подается в распылитель и распределяется равномерно по поверхности стружек. Стекая по стружкам, этиловый спирт, содержащийся в сусле, постепенно превращается в уксусную кислоту. Затем полусброженное сусло снова охлаждается, накачивается насосом в верхнюю часть биореактора и распыляется еще раз. Эта операция повторяется до тех пор, пока содержание уксусной кислоты в жидкости не достигнет 10,5 %. Готовый продукт сливают, оставляя в генераторе лишь незначительную часть (10 %). Остающийся уксус служит для питания микробов, а также для того, чтобы насос мог нормально продолжать работать. После этого в генератор быстро вводят новую партию свежего сусла. Чтобы уксусное брожение протекало нормально, сахар, содержащиеся в сбраживаемом субстрате должен быть превращен в этиловый спирт, поэтому уксуснокислому брожению предшествует спиртовое. Уксус, полученный микробиологическим путем, различают по сортам в зависимости от характера сбраживаемого субстрата. Известен яблочный, виноградный, грушевый и другие сорта уксуса. Уксус, полученный при брожении, имеет приятный аромат и вкус, которые обуславливают побочные продукты брожения: сложные эфиры, высшие спирты, органические кислоты.
Процесс идет в анаэробных условиях в режиме непрерывного культивирования продуцента. Для роста бактерии Acetobacter aceti используют питательные среды, содержащие 6 - 12 %этилового спирта, 1 % бактериального гидролизата, 0,05 % дигидрофосфата калия, 0,1 % гидрофосфата аммония и 0,05% сульфата магния. Максимальная удельная активность непрерывной культуры A. aceti (количество микрограммов субстрата, подвергшегося окислению 1мкг биомассы за 1 мин) достигается к 20-м суткам культивирования при концентрации спирта 7 % и составляет 3,0 ед./мг.Установлено, что продуцент уксусной кислоты из рода Acetobacter, развиваясь на поверхности среды, образует слизистую пленку, которая состоит из целлюлозы (90 %) и клеток бактерий. Если эту пленку снять, высушить и соответственно обработать, можно получить достаточно прочные биофильтры медицинского назначения. Если ожоговые раны покрыть такими биофильтрами, они заживают в течении 7- 8 суток. В настоящее время процесс реализуют как поверхностным, так и глубинным способом. Поверхностный режим протекает в струйных генераторах, наполненных древесной стружкой, объемом до 60 м3. Исходный питательный раствор с бактериями распыляют по поверхности стружек, и он стекает, собираясь в нижней части аппарата. После этого жидкость собирают и вновь закачивают в верхнюю часть аппарата. Процедуру повторяют 3–4 раза, в результате в течение 3-х дней до 90 % спирта трансформируется в ацетат. Этот старый способ протекает более эффективно и равномерно в генераторах Фрингса с автоматическим поддержанием температуры и принудительной подачей воздуха. По такой технологии производят до 400 млн л уксусной кислоты в год. Современные промышленные процессы получения уксуса реализуют в глубинной культуре в специальных аэрационных аппаратах с термостабилизацией и механической системой пеногашения. Скорость аэрации составляет 3.4 м3/м3×ч., вращение ротора – 1500 об./мин., температура 30°С. Исходная инокулируемая смесь содержит этанол и уксусную кислоту, соответственно, около 5 и 7 %; конечная концентрация уксуса через 1.5 суток составляет 12–13 %. Процесс – полупроточный, отливно-доливный. Каждые 30–35 часов до 60 % культуры заменяют на свежее сусло. При глубинной ферментации выход продукта на 1 м3 в 10 раз выше по сравнению с поверхностной ферментацией. К началу 90-х гг. таким способом производили до 715 млн. литров 10 % уксусной кислоты в год. Разработан и реализован эффективный непрерывный способ получения уксусной кислоты в батарее последовательно работающих ферментеров (обычно 5 аппаратов). Температура культивирования составляет 28° для Acetobacter и 35° при использовании в качестве продуцента культуры Bact. schutzenbachii. Наилучшим сырьем для процесса является этиловый спирт, полученный из зерно-картофельного сырья, при его концентрации около 10 %. Оптимум рН для развития бактерий – около 3. При увеличении содержания уксусной кислоты в культуре свыше 8 % рост бактерий замедляется, при 12–14 % прекращается. Поэтому процесс проводят в батарее последовательно соединенных аппаратов. Первый выполняет роль инокулятора, поэтому в него непрерывно подают свежую среду и поддерживают условия, оптимальные для быстрого образования биомассы бактерий. Культура из первого аппарата поступает во второй аппарат и далее – в последующие, при этом транспортировка культуральной жидкости осуществляется воздухом. В каждом аппарате условия ферментации стабилизируются в соответствии с требованиями течения хода ферментации, при постепенном понижении температура среды от 28° в первом аппарате до 25° – в последнем. Режим аэрации также изменяется, от 0.4 до 0.15 м3/м3 мин. Концентрация спирта со второго по четвертый аппарат стабилизируется на требуемом уровне подачей в них среды с 40 % этанолом. Из последнего аппарата выводится культуральная жидкость с содержанием ацетата не ниже 9.0 и не выше 9.3 %. Выход кислоты составляет до 90 кг из 100 л безводного спирта. На постферментационной стадии после отделения бактериальной биомассы раствор уксуса фильтруют, освобождая от окрашенных и взвешенных частиц, и далее подвергают пастеризации. Для повышения концентрации исходные растворы вымораживают до 20–30 %. Дальнейшее концентрирование до получения ледяной уксусной кислоты (98.0–99.8 %), проводят методом перегонки. Уксус, полученный микробиологическим путем, различают по сортам в зависимости от характера сбраживаемого субстрата. Известен яблочный, виноградный, грушевый и другие сорта уксуса. Уксус, полученный при брожении, имеет приятный аромат и вкус, которые обуславливают побочные продукты брожения: сложные эфиры, высшие спирты, органические кислоты.
Производство итаконовой кислоты
Процесс синтеза итаконовой кислоты очень похож на соответствующий процесс получения лимонной кислоты. Она может быть получена методами поверхностного и глубинного культивирования. Чаще используется глубинный метод. Процесс включает культивирование продуцента на среде с высокой концентрацией сахара в условиях ограничения роста гриба минеральными компонентами среды (обычно железом и фосфором), при низким рН среды и достаточном обеспечении кислородом. Итаконовая кислота в отличие от лимонной кислоты является токсичным продуктом. При концентрации ее в среде около 70 г/л наблюдается угнетение роста продуцента и синтеза продукта. Избежать токсичного действия накапливающиеся кислоты можно нейтрализацией ее NH4OH. Периодическое введение NH4OH и поддержание значение рН среды на уровне 3,8 обеспечивает накопление до 150-200 г итаконовой кислоты в литре раствора. Другая особенность процесса синтеза итаконовой кислоты с помощью A. terreus – необходимость внесения в среду высокой концентраций ионов таких металлов, как Zn2+, Mg2+ и Cu2+. В результате многоступенчатой обработки природного штамма мутагенами и последующего отбора селекционированных ряд высокоактивных мутантов A. terreus используется для производства итаконовой кислоты во всех производствах. В качестве посевного материала при поверхностным и глубинным методах ферментации в промышленностях используют сухие конидии гриба, отделенные от мицелия и смешанные с активированным углем. При поверхностным способе процесс ферментации осуществляется в кюветах по бессменному варианту без долива или с доливом. В качестве источника углерода используют свекловичную мелассу или продукт переработки отходов древесины – двойное соединение глюкозы с NaCl. Рациональная концентрация сахара 8%, кроме того, среда содержит NH4NO3, MgSO4, ZnSO4·7H2O, K4Fe(CN)6 и кукурузный экстракт. Начальное рН среды 5,0. важным фактором является воздушный режим в «бродильном камере». При глубинном способе процесс осуществляется последовательно в двух ферментаторах. Среда в посевном ферментаторе засевается спорами гриба. В конечной фазе роста мицелий передается из посевного в основной аппарат. Ферментационная среда содержит 6-7% сахара мелассы (состав солей тот же, что и при поверхностном методе), рН среды поддерживается на уровне 2,1 – 2,3, оптимальном для синтеза итаконовой кислоты. В течении ферментации осуществляется интенсивное перемешивание и аэрация среды. В конце процесса концентрация кислоты достигает 40-60 г/л. Биосинтез итаконовой кислоты в глубинных условиях происходит намного интенсивнее, чем в поверхностных. Содержание итаконовой кислоты достигает 15–20 %, остаточная концентрация сахаров не превышает 0.6 %. В отличие от лимонной, итаконовая кислота – токсичный продукт, при ее концентрации около 7 % рост продуцента угнетается, и скорость продукции кислоты снижается. Токсичность итаконовой кислоты нейтрализуют дробными добавками гидроксиаммония, рН среды при этом стабилизируется на уровне 3.5–3.8. При глубинной ферментации конечная концентрация итаконовой кислоты ниже, 4–6 %. Товарный продукт – кристаллическая итаконовая кислота 92 % содержания, остальное – влага (3–6 %) и другие кислоты. Среды содержат высокие концентрации сахаров, обычно используют мелассу, при дефиците фосфора и железа. Особенностью процесса получения данной кислоты является высокая потребность продуцента в солях цинка, магния и меди. При поверхностной ферментации в течение 10–12 суток образуется около 60 % продукта в пересчете на сахар, доля целевой кислоты в смеси (синтезируются также янтарная, щавелевая и фумаровая кислоты) – свыше 90%. После окончания процесса ферментации культуральную среду освобождают от мицелия, осветляют активированным углем и упаривают под вакуумом. Итаконовая кислота кристаллизируется из упаренного раствора. Перекристаллизированная Итаконовая кислота используются для химических синтезов.
Производство молочной кислоты
Промышленное производство молочной кислоты начато в конце ХIХ века с участием молочнокислых бактерий Lactobacillus delbrueckii, L. leichmannii, L.bulgaricus. Образование молочной кислоты из глюкозы возможно несколькими путями. При сбраживании гомоферментными молочнокислыми бактериями:
С6Н12О6 ® 2 СН2ОН2СНОНСНО (глицеральдегид) ®
® 2 СН3СОСНО (метилглиоксаль) + 2 Н2О,
СН3СОСНО (метилглиоксаль) + Н2О ® СН3СНОНСООН(молочная кислота).
Второй путь, гетероферментный, включает распад глюкозы до пировиноградной кислоты и восстановление последней до молочной кислоты:
С6Н12О6 ® СН3СОСООН + Н2 ® СН3СНОНСООН.
Молочнокислое брожение протекает в анаэробных условиях, однако лактобациллы относятся к факультативным анаэробам, поэтому при ферментации воздух полностью не удаляют из ферментеров. В качестве сырья используют сахарную и тростниковую мелассу и гидролизаты крахмала, при этом концентрация сахаров в исходной среде в зависимости от характера брожения составляет примерно от 5 до 20 %. Используют восстановленные формы азота, сульфаты или фосфаты аммония, а также солод и кукурузный экстракт в качестве источника факторов роста. Молочной, или казеиновой, сывороткой называют жидкость, остающуюся после удаления из молока жиров и казеина. Она содержит некоторое количество белков (лактальбумина), 4,6 % лактозы, рибофлавин, минеральные соли и воду. Молочная сыворотка служит питательным субстратом для молочнокислых бактерий в производстве молочной кислоты. Пастеризованную сыворотку засевают закваской, содержащей Lactobacillus bulgaricus. Образующаяся по ходу брожения молочная кислота периодически нейтрализуется известью. По окончании брожения раствор нагревают для удаления лактальбумина. После осаждения свернувшегося лактальбумина раствор молочнокислого кальция сливается, фильтруется, обрабатывается для осветления активированным углем, снова фильтруется и, наконец, упаривается. Молочнокислый кальций кристаллизуется, кристаллы отмывают и в случае необходимости подвергают дальнейшей очистке, а затем высушиванию. Готовый продукт поступает в продажу в виде молочнокислого кальция или молочной кислоты. Возможно использование сульфитного щелока с участием бактерий L. delbrueckii. Ферментацию проводят в глубинной культуре при рН 6.3–6.5 и строго постоянной температуре 50°С. Длительность процесса составляет до 7–11 суток. В ходе процесса брожения для коррекции изменяющегося рН в культуру вносят мел, 3–4 раза в течение суток. Конечная концентрация образующегося лактата кальция составляет 10–15 %, остаточная концентрация сахаров – 0.5–0.7 %. На стадии получения готового продукта культуральную среду нагревают до 80–90°, затем нейтрализуют гашеной известью до слабощелочной реакции. После отстаивания в течение 3–5 ч взвешенные частицы декантируют. После этого раствор лактата кальция подают на фильтр-пресс. Фильтрат упаривают до концентрации 27–30 %, охлаждают до 25–30° и подвергают кристаллизации. Промытый лактат кальция отделяют центрифугированием и подвергают расщеплению серной кислотой при 60–70°. Сырую молочную кислоту 18–20 % концентрации упаривают в несколько этапов в вакуум-выпарных аппаратах до 70 % концентрации. Отфильтрованную кислоту после фильтр-пресса подают на розлив с внесением небольших количеств мела, при этом около 10 % кислоты превращается в кристаллический лактат, который связывает молочную кислоту.
Новые возможности для интенсификации производственных процессов получения органических кислот открывает применение иммобилизованных ферментов и клеток микроорганизмов.
Лекция 8. Получение белка. Получение белков из дрожжей. Получение белков из фототрофных микроорганизмов. Культура микроводорослей и цианобактерий. Пищевая ценность и перспективы применения микробного белка.
Получение белка. Получение белков из дрожжей
Микроорганизмы начали использовать в производстве белковых продуктов задолго до возникновения микробиологии. Достаточно упомянуть всевозможные разновидности сыра, а также продукты, получаемые путем ферментации соевых бобов. И в первом, и во втором случае питательной основой является белок. При выработке этих продуктов при участии микробов происходит глубокое изменение свойств белоксодержащего сырья. В результате получают пищевые продукты, которые можно дольше хранить (сыр) или удобнее потреблять (соевый творог). Микробы играют роль в производстве некоторых мясных продуктов, предназначенных для хранения. Так, при изготовлении некоторых сортов колбасы используется кислотное брожение, обычно при участии комплекса молочнокислых бактерий. Образовавшаяся кислота способствует сохранности продукта и вносит вклад в формирование его особого вкуса.Этим, пожалуй, и ограничивается использование микроорганизмов в переработке белков. Возможности современной биотехнологии в этих производствах невелики, за исключением сыроделия. Другое дело – выращивание и сбор микробной массы, перерабатываемой в пищевые продукты: здесь биотехнология может проявить себя во всей полноте.
По многим важным показателям биомасса микроорганизмов может обладать весьма высокой питательной ценностью. В немалой степени эта ценность определяется белками: у большинства видов они составляют значительную долю сухой массы клеток. На протяжении десятилетий активно обсуждаются и исследуются перспективы увеличения доли белка микроорганизмов в общем балансе производимого во всем мире белка.
Производство такого белка связано с крупномасштабным выращиванием определенных микроорганизмов, которые собирают и перерабатывают в пищевые продукты. Чтобы осуществить возможно более полное превращение субстрата в биомассу микробов, требуется многосторонний подход. Выращивание микробов в пищевых целях представляет интерес по двум причинам. Во-первых, они растут гораздо быстрее, чем растения и животные: время удвоения их численности измеряется часами. Это сокращает сроки, нужные для производства определенного количества пищи. Во-вторых, в зависимости от выращиваемых микроорганизмов в качестве субстратов могут использоваться разнообразные виды сырья. Что касается субстратов, то здесь можно идти по двум главным направлениям: перерабатывать низкокачественные бросовые продукты или ориентироваться на легкодоступные углеводы и получать за их счет микробную биомассу, содержащую высококачественный белок.
| <== предыдущая страница | | | следующая страница ==> |
| Введение 6 страница | | | Введение 8 страница |
Дата добавления: 2014-02-27; просмотров: 1667; Нарушение авторских прав

Мы поможем в написании ваших работ!