
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Строение молекулы белка
Белки – этот высокомолекулярные азотсодержащие соединения, состоящие из аминокислот. В состав белков входят сотни остатков аминокислот. Однако все белки, независимо от происхождения образуются 20 видами аминокислот. Поэтому эти 20 аминокислот называют протеиногенными.
α-Аминокислоты представляют собой производные карбоновых кислот, у которых один водородный атом, у α-углерода, замещен на аминогруппу (—NH2), например:
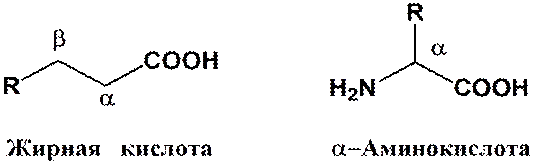
Следует подчеркнуть, что все аминокислоты, входящие в состав природных белков, являются α-аминокислотами, хотя аминогруппа в свободных аминокарбоновых кислотах может находиться в β-, γ-, δ-и ε-положениях.
Аминокислоты — это гетеро-функциональные соединения. В молекуле аминокислоты содержится несколько функциональных (определяющих их свойства) групп: аминогруппа —NH2, карбоксильная группа —СООН и радикалы (остатки) —R, имеющие различное строение:
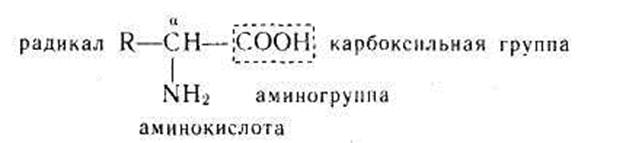
Аминокислоты содержат карбоксильную группу COOHи аминогруппу NH2.Правда, некоторые белки все же содержат в очень малых количествах аминокислоты, не входящие в состав протеиногенных. Такие аминокислоты называют минорными.Они образуются из протеиногенных аминокислот после завершения синтеза белковых молекул.
Число функциональных групп может быть различным: моно-аминомонокарбоновые, диаминомонокарбоновые, моноаминодикарбоновые аминокислоты и т. д. По строению боковых цепей (полярности, заряженности) аминокислоты группируются на неполярные (гидрофобные), полярные (гидрофильные), но не заряженные, и полярные, имеющие положительный или отрицательный заряд.


| <== предыдущая страница | | | следующая страница ==> |
| Биологическая роль белков | | | Ароматические R-группы |
Дата добавления: 2014-03-11; просмотров: 1034; Нарушение авторских прав

Мы поможем в написании ваших работ!