
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
НЕОБРАТИМЫХ ПРОЦЕССОВ
ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ ДЛЯ ОБРАТИМЫХ И
Представим, что система переходит из начального состояния в конечное двумя путями - обратимо и необратимо.
Qобр = DU + Wобр
Qнеобр = DU + Wнеобр
т.к. величина ΔU определяется только начальным и конечным состоянием системы и поэтому одинаковы в обоих процессах.
Wнеобр < Wобр
следовательно Qнеобр < Qобр
Для обратимого процесса
dQобр = TdS
dS = 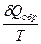
DS = S2 – S1 = 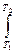
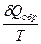
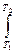
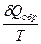 = 0
= 0
dS = 0
DS = 0
Для необратимого процесса
dQнеобр < TdS
dS > 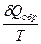
DS > 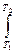
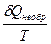
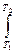
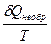 < 0
< 0
dS > 0
DS > 0
TdS ³dU + dW
TdS ³ dU + PdV
При протекании в изолированной системе обратимого процесса энтропия системы остается постоянной
DS = 0
Если в ней будет протекать неравновесный процесс, то энтропия будет возрастать
DS > 0
В общем случае в изолированной системе
DS ³ 0
Исследуя энтропию, очевидно можно предсказывать направление процесса. Если в изолированной системе для какого-либо процесса энтропия возрастает, то процесс возможен (может протекать самопроизвольно),если энтропия согласно расчета должна убывать, то процесс невозможен. При постоянстве энтропии процесс равновесен.
Причем при равновесии энтропия достигает максимально возможного значения.
| <== предыдущая страница | | | следующая страница ==> |
| ЭНТРОПИЯ | | | ИЗМЕНЕНИЕ ЭНТРОПИИ В РАЗЛИЧНЫХ ПРОЦЕССАХ |
Дата добавления: 2014-03-11; просмотров: 293; Нарушение авторских прав

Мы поможем в написании ваших работ!