
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Лекция № 4.ФЕРМЕНТЫ (продолжение)
1.СВОЙСТВА ФЕРМЕНТОВ.
2.МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ.
З.МОЛЕКУЛЯРНЫЕ ЭФФЕКТЫ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ.
СВОЙСТВА ФЕРМЕНТОВ.
1 .Высокая каталитическая активность. УРЕАЗА повышает скорость реакции в 10 раз.
2.Ферменты, являясь белками, проявляют ТЕРМОЛАБИЛЬНЫЕ свойства - чувствительность к изменению температуры.
При повышении температуры на каждые 10 градусов, скорость ферментативных реакций повышает в 1,5-2 раза (правило ВАНТ - ГОФФА). Это правило применимо для ферментов в очень узком интервале температуры, т.к. уже при 50-60 градусах наблюдается денатурация, а при 100 гр. - полная денатурация с потерей активности. При 1-3 гр. Активность фермента также понижается, но при понижении температуры структура его сохраняется, поэтому при последующем повышении Т. активность восстанавливается. Это свойство используется в клинической практике при проведении оперативных вмешательств. Температура, при которой фермент проявляет максимальную активность, называется ОПТИМАЛЬНОЙ.

3.Ферменты чувствительны к изменениям РН среды. Для большинства ферментов оптимальные значения РН лежат в нейтральной среде (для КАТАЛАЗЫ РН=7).
Есть ферменты, для которых оптимальные значения РН лежат в кислой среде (пепсин РН=1,5-2,5). Некоторые ферменты проявляют активность в щелочной среде (АРГИНАЗА РН=10-11). Изменения РН приводит к изменению степени ионизации кислых и основных групп в активном центре фермента, т.к. эти группы участвуют в связывании субстрата и его превращении. Изменение РН приводит к конформационной перестройке не только активного центра фермента, но и всей молекулы фермента. Это может сопровождаться нарушением третичной структуры фермента. При оптимальном значении РН функциональные группы активного центра находятся в наиболее реакционно-способном состоянии, и это обеспечивает образование фермент-субстратного комплекса.
4.Специфичность действия ферментов. В основе специфичности действия ферментов лежит КОНФОРМАЦИОННОЕ соответствие его активного центра молекуле субстрата. Различают следующие виды специфичности:
А). Абсолютная специфичность. Ей обладают ферменты, которые действуют только на 1 субстрат и не действуют на другие субстраты.
УРЕАЗА ГИДРОЛИЗУЕТ МОЧЕВИНУЮ.
АРГИНАЗА ОТЩЕПЛЯЕТ АРГ.
ФУМАРАЗА - ГИДРАТАЦИЯ ФУМАРОВОЙ КИСЛОТЫ.
В). СТЕРИОСПЕЦИФИЧНОСТЬ. Ей обладают ферменты, действующие на пространственные или стереоизомеры. ЦИС и ТРАНС изомеры; оптические изомеры (ЭНАНТИОМЕРЫ).
С). Групповая специфичность. Ей обладают ферменты, которые катализируют однотипные реакции сходных по строению субстратов, т.е. эти субстраты могут содержать в своём составе одинаковые группы атомов.
Пример: ЛИПАЗА - участвует в расщеплении ЛИПИДОВ, содержащих в своём
составе СЛОЖНОЭФИРНУЮ связь.
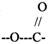
ПЕПТИДАЗЫ действуют на субстраты, содержащие ПЕПТИДНЫЕ связи.
Их действию подвергаются ПЕПТИДЫ,Б.
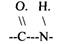
МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ.
С термодинамической точки зрения, действие любого фермента направлено на понижение энергии активации. Энергия активации - это то дополнительное количество энергии, которое нужно сообщить молекуле, чтобы перевести её из неактивного состояния в состояние активности. Чем ниже энергия активации, тем выше скорость реакции. Теория действия ферментов была предложена БЕЙЛИСОМ и ВАНБУРГОМ. Эта теория получила название АДСОРБЦИОНОЙ. Согласно ей, фермент представляет собой "губку", которая адсорбирует на своей поверхности молекулы реагирующих веществ. Она как бы стабилизирует их, способствует взаимодействию. Эта гипотеза не могла объяснить специфичность действия ферментов. 70 лет назад была предложена др. теория МИХАЭЛИСОМ и МЕНТЕНОМ. Они выдвинули понятие о F-S комплексе. Фермент взаимодействует с субстратом, образуя нестойкий промежуточный F-S комплекс, который затем распадается с образованием продуктов реакции (Р) и освобождением фермента. В этом процессе выделяют несколько стадий:
1.Диффузия S к F и их СТЕРИЧЕСКОЕ взаимодействие с образованием F-S комплекса. Эта стадия не продолжительна. Её скорость зависит от концентрации субстрата и скорости диффузии его к активному центру фермента. На этой стадии практически не происходит понижения энергии активации.

2.Преобразование F-S комплекса в один, или несколько, активированных комплексов.
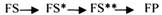
Они называются переходными. Эта стадия является наиболее продолжительной по времени. При этом происходит разрыв связей в молекуле субстрата, образование новых связей, т.е. образуются Р реакции. Е активации ¯.
3.Освобождение продуктов реакции от фермента и поступление их в окружающую среду.

МОЛЕКУЛЯРНЫЕ ЭФФЕК ТЫ ФЕРМЕНТАТИВНОГО ДЕЙСТВИЯ.
1. Эффект концентрации. Чтобы произошло взаимодействие между молекулами реагирующих веществ, они должны обязательно столкнуться. В обычных условиях без участия фермента столкновение этих молекул является медленным, что замедляет реакцию. Поэтому основная роль ферментов заключается в притяжении молекул реагирующих веществ на свою поверхность и концентрация этих молекул в области активного центра фермента.
2. Эффект, сближения и ориентации. Это характерное свойство ферментов, которое позволяет ускорить превращение субстрата и повышение скорости реакции в 1000 и 10000 раз. Контактные участки активного центра фермента связывают специфически молекулы субстрата, сближают их и обеспечивают взаимную ориентацию так, чтобы это было выгодно для действия каталитических групп фермента. Такое упорядоченное расположение S приводит к снижению энергии активации.
3. Эффект натяжения ("дыбы"). До присоединения субстрата к активному центру фермента, его молекула как бы в расслабленном состоянии. После связывания молекула субстрата растягивается и принимает напряжённую деформированную конфигурацию. При этом увеличивается длина межатомных связей, следовательно, понижается Е активации.
4. Кислотно-основной катализ. В активном центре фермента содержатся группы кислотного и основного типа. Группы кислотного типа отщепляют Н+ и имеют отрицательный заряд. Группы основного типа присоединяют Н+ и имеют положительный заряд. Кроме основных групп, положительный заряд несут ионы металлов. После связывания субстрата с активным центром фермента, молекулы субстрата перестраиваются, т.к. они подвергаются действию каталитических групп активного центра: одни группы присоединяют Н+, др. его отщепляют. Это приводит к ускорению образования продукта реакции, т.е. способствует понижению энергии активации.
5.Ковалентный катализ (ФОСФОТАЗЫ). Наблюдается у ферментов, которые образуют ковалентные связи между каталитическими группами активного центра и субстрата. В результате формируется промежуточный F-S комплекс, который неустойчив, легко распадается, продукты реакции быстро освобождаются. 6.Эффект индуцированного соответствия.
Он объясняет специфичность действия ферментов. По этому поводу имеется 2 точки зрения:
А). Гипотеза ФИШЕРА. Согласно ей имеется строгое СТЕРИЧЕСКОЕ соответствие субстрата и активного центра фермента. По ФИШЕРУ, фермент - это жёсткая структура, а субстрат является как бы слепком его активного центра. Если субстрат подходит к активному центру фермента как ключ к замку, то реакция возможна. Но эта теория не могла объяснить групповую специфичность фермента.
В). Теория индуцированного соответствия КОШЛЕНДА дополнила теорию ФИШЕРА. Согласно ей молекула фермента - это не жёсткая, а гибкая структура. После связывания фермента с субстратом, изменяется КОНФОРМАЦИЯ активного центра фермента и всей молекулы субстрата. Они находятся в состоянии индуцированного соответствия. Это происходит в момент взаимодействия. Гипотеза КОТЛЕНДА получила название "рука-перчатка".
| <== предыдущая страница | | | следующая страница ==> |
| Лекция № 3. ФЕРМЕНТЫ (F) | | | Лекция № 5. ФЕРМЕНТЫ (продолжение) |
Дата добавления: 2014-04-15; просмотров: 883; Нарушение авторских прав

Мы поможем в написании ваших работ!