
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Основные стехиометрические законы химии
Стехиометрия – раздел химии, рассматривающий количественные соотношения между реагирующими веществами.
Закон сохранения массы: масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции.
Закон постоянства состава: всякое чистое вещество, независимо от способа его получения, имеет постоянный качественный и количественный состав.
Закон применим только к соединениям с молекулярной структурой.
Закон эквивалентов: массы реагирующих друг с другом веществ, а также массы продуктов этой реакции пропорциональны молярным массам эквивалентов этих веществ.
Например, в условной реакции А + 2В = 3С + Д
mА : mВ : mС : mД = ЭА : ЭВ : ЭС : ЭД,
где m – масса веществ, а Э – молярная масса эквивалентов.
Другими словами можно сказать, что вещества реагируют и образуются в эквивалентных количествах. Один эквивалент одного вещества всегда взаимодействует с одним эквивалентом другого.
Эквивалент – реальная или условная частица, которая может присоединять, высвобождать или быть каким–либо другим образом эквивалентна одному иону водорода в кислотно–основных реакциях или одному электрону в окислительно–восстановительных реакциях.
При использовании понятия «эквивалент» всегда необходимо указывать, к какой ионной реакции оно относится.
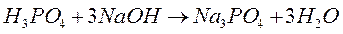
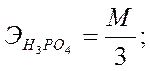
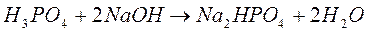
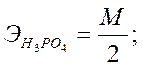
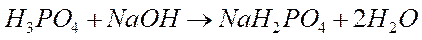
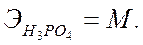
| <== предыдущая страница | | | следующая страница ==> |
| Электродные потенциалы. Электродвижущие силы. Электролиз | | | Законы газового состояния |
Дата добавления: 2014-04-24; просмотров: 546; Нарушение авторских прав

Мы поможем в написании ваших работ!