
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Способы выражения концентраций раствора
| Способ выражения концентрации | Математическое выражение | Расчетная формула |
1. Процентная концентрация или массовая доля
Обозначается 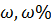
| 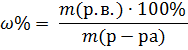
|
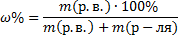
|
2. Молярная концентрация или молярность
Обозначается 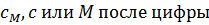 .
Примеры. 1M H2SO4 – одномолярный раствор серной кислоты;
0,1М – децимолярный р-р;
0,01М – сантимолярный;
0.001М - миллимолярный .
Примеры. 1M H2SO4 – одномолярный раствор серной кислоты;
0,1М – децимолярный р-р;
0,01М – сантимолярный;
0.001М - миллимолярный
| 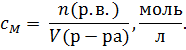 Если
Если 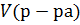 = 1 л, = 1 л, 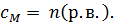 Молярная концентрация показывает, сколько молей растворенного вещества содержится в одном литре раствора
Молярная концентрация показывает, сколько молей растворенного вещества содержится в одном литре раствора
|
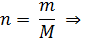
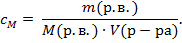
|
3. Нормальная концентрация или нормальность
Обозначается 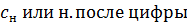 .
Пример. 1н. NaOH – однонормальный раствор гидроксида натрия;
0,1н. – децинормальный р-р;
0,01н. – сантинормальный;
0.001н. - миллинормальный .
Пример. 1н. NaOH – однонормальный раствор гидроксида натрия;
0,1н. – децинормальный р-р;
0,01н. – сантинормальный;
0.001н. - миллинормальный
| 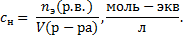 Если
Если 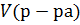 = 1 л, = 1 л, 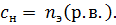 Нормальная концентрация показывает, сколько молей эквивалентов растворенного вещест-ва содержится в одном литре раствора
Нормальная концентрация показывает, сколько молей эквивалентов растворенного вещест-ва содержится в одном литре раствора
|
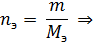
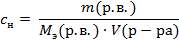
|
| 4. Молярная (мольная) доля Обозначается x или N | 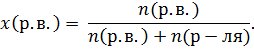
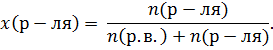
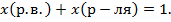
| 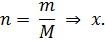
|
5. Моляльная концентрация или моляльность.
Обозначается 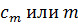
|
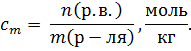 Если
Если 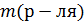 = 1 кг, = 1 кг, 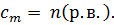 Моляльная концентрация показывает, сколько молей растворенного вещества приходится на один литр раствори-теля
Моляльная концентрация показывает, сколько молей растворенного вещества приходится на один литр раствори-теля
|
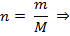
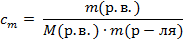
|
Задача 1. К 8 л воды добавили 2 л этилового спирта плотностью 0,8 г/мл. Рассчитать моляльную концентрацию раствора.
Решение. Расчет ведем по формуле:
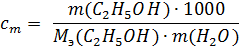
1) 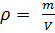 ⇒
⇒ 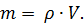
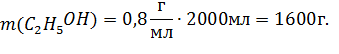
2) M( 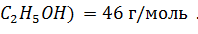
3) m( 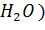 = 8000 г (так как
= 8000 г (так как 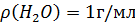 ).
).
4) m =  = 4,35 моль/1000 г
= 4,35 моль/1000 г 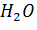 .
.
| <== предыдущая страница | | | следующая страница ==> |
| Общие сведения о растворах | | | Теория растворов |
Дата добавления: 2014-05-03; просмотров: 402; Нарушение авторских прав

Мы поможем в написании ваших работ!