
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Аналитические выражения для работы и теплоты в процессе Теплоемкость
Вычисление работы.
Для количественной меры механического взаимодействия рабочего тела с окружающей средой, то есть механической работы против внешних сил в термодинамическом процессе, отнесенной к 1 кг вещества, из курса физики известно выражение
dl = pdv,
где р – абсолютное давление рабочего тела, Па.
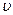 – удельный объем, м3/кг.
– удельный объем, м3/кг.
Для конечного процесса, в которой объем изменяется от 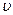 1 до
1 до 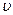 2, общее выражение для механической работы принимает вид:
2, общее выражение для механической работы принимает вид:
 .
.
В общем случае давление (р) величина переменная, зависящая от удельного объема ( 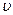 ). Для вычисления механической работы процесса должна быть известна зависимость между давлением (р) и удельным объемом (
). Для вычисления механической работы процесса должна быть известна зависимость между давлением (р) и удельным объемом ( 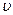 ) в данном процессе, то есть должно быть задано уравнение процесса - р=f(
) в данном процессе, то есть должно быть задано уравнение процесса - р=f( 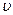 ). Графически эта зависимость может быть изображена в «р –
). Графически эта зависимость может быть изображена в «р – 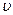 » координатах.
» координатах.
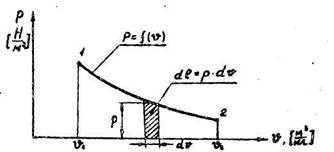
Рис. 1.6. К вычислению механической работы в термодинамическом процессе.
Очевидно, величина работы будет зависеть от характера кривой процесса и изображается в «р – 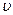 » координатах площадью, ограниченной кривой процесса, двумя ординатами и осью абсцисс, то есть
» координатах площадью, ограниченной кривой процесса, двумя ординатами и осью абсцисс, то есть
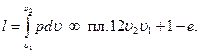
Так как абсолютное давление величина всегда положительная (р>0), то знак работы будет тем же, что и у изменения объема (- dv).
При расширении газа dv.> 0 и l >0.
При сжатии газа dv<0 и l <0.
Вычисление количества теплоты
Количественную меру термического (теплового) взаимодействия рабочего тела с окружающей средой - количество теплоты - можно найти различными способами. Один из способов вычисления количества теплоты связан с понятием энтропии.
Изменение энтропии в термодинамическом процессе, отнесенное к 1 кг вещества, равно
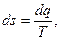
откуда
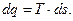

Рис.1.7. К вычислению количества теплоты
в термодинамическом процессе.
Абсолютная температура (Т) - величина всегда положительная, следовательно, знак количества теплоты (q) определяется знаком изменения энтропии (ds): отвод тепла (q<0) происходит при убывании энтропии (ds<0), а подвод тепла (q>0) происходит при возрастании энтропии (ds>0).
Второй способ вычисления количества теплоты связан с понятием теплоемкости рабочего тела в термодинамическом процессе, известного из курса физики:
с=dq/dt,
где dq - элементарное количество теплоты, подведенное в термодинамическом процессе, Дж/кг;
dt - элементарное изменение температуры, вызванное подводом или отводом элементарного количества теплоты.
В зависимости от выбранной количественной меры рабочего тела различают следующие виды теплоемкости: массовая - с, объемная - 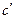 , молярная -
, молярная - 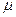 с.
с.
Массовая теплоемкость (с) - теплоемкость 1 кг рабочего тела в термодинамическом процессе; Дж/кгК.
Объемная теплоемкость ( 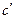 ) - теплоемкость 1 м3 рабочего тела, взятого при нормальных условиях; Дж/ м3 К.
) - теплоемкость 1 м3 рабочего тела, взятого при нормальных условиях; Дж/ м3 К.
Молярная теплоемкость ( 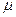 с) - теплоемкость I киломоля рабочего тела в термодинамическом процессе; Дж/кмольК.
с) - теплоемкость I киломоля рабочего тела в термодинамическом процессе; Дж/кмольК.
Соотношение между различными видами теплоемкости
1 киломоль рабочего тела имеет массу, равную кг, следовательно:
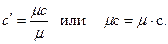
1 киломоль рабочего тела (газа) при нормальных физических условиях имеет объем 22,4 м3.Отсюда
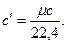
Зависимость теплоемкости от процесса
В термодинамических расчетах большое значение имеет теплоемкости рабочего тела при нагреве (охлаждении) в условиях постоянного объема ( 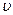 =const)и при постоянном давлении (р=const)
=const)и при постоянном давлении (р=const)
При теплообмене и в условиях постоянного объема теплоемкость носит название изохорной и определяется следующим образом:
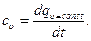
При нагреве газа в условиях постоянного объема все количество теплоты идет на изменение внутренней анергии рабочего тела, так как отсутствует энергообмен в виде механической работы (d 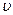 = 0).
= 0).
Если же процесс теплообмена происходит при постоянном давлении (р=сonst), то теплоемкость носит название изобарной и определяется по зависимости
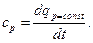
При нагревании газа в условиях постоянного давления, кроме увеличения внутренней энергии, совершается механическая работа расширения газа - 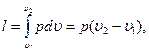 следовательно, для нагрева рабочего тела в одном и том же интервале температур в изохорном процессе потребуется меньше количество теплоты, чем в изобарном процессе, то есть ср > с
следовательно, для нагрева рабочего тела в одном и том же интервале температур в изохорном процессе потребуется меньше количество теплоты, чем в изобарном процессе, то есть ср > с 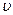 .
.
Соотношение между ср и с 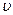 .
.
В термодинамических расчетах часто встречается отношение теплоемкостей - 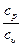 , поэтому для упрощения записей это соотношение обозначили специальным образом – k– показатель адиабаты.
, поэтому для упрощения записей это соотношение обозначили специальным образом – k– показатель адиабаты.
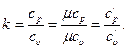
Величина коэффициента «k» зависит только от природы газа, его физических свойств и состояния, то есть является физической константой. Величина соотношения между теплоемкостями имеет следующие значения:
-для одноатомных газов -k = 1.69;
-для двухатомных газов -k= 1,4;
-для трехатомных газов - k = 1,33.
Уравнение Майера
Уравнение Майера записывается в одной из двух форм:
ср = с 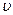 +R или ср - с
+R или ср - с 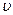 = R.
= R.
Уравнение Майера показывает, что подводимое количество теплоты при нагревании идеального газа в условиях постоянного давления расходуется на увеличение внутренней энергии и на совершение механической работы.
Из уравнения Майера получаем выражение для изохорной и изобарной теплоемкостей:
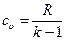 и
и 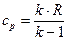
| <== предыдущая страница | | | следующая страница ==> |
| Термические параметры состояния. Уравнение состояния | | | Первый закон термодинамики. Закон сохранения и превращения энергии |
Дата добавления: 2014-10-28; просмотров: 834; Нарушение авторских прав

Мы поможем в написании ваших работ!