
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Переход жидкость – пар
В рассматриваемом случае переходов жидкость – пар в справочниках приводятся данные для самых разных условий переходов. Чтобы соотнести величины, характеризующие переход из жидкости в пар, нужно привести начальные (жидкость) и конечные (пар) условия для разных веществ к одинаковым отношениям концентраций молекул.
Атомы всех элементов близки друг к другу по размерам D = 2Å – 4Å. Следовательно, отношение концентраций молекул для разных веществ, находящихся в конденсированном состоянии при низких температурах, лежит в диапазоне 1 – 8. Нужно учесть это обстоятельство и, соответственно, подобрать нужную температуру для каждого вещества. В приведенной ниже таблице все вещества в твердом состоянии образуют кубическую гранецентрированную решетку. Подбор температур осуществлялся так, чтобы отношение давления насыщенного пара вещества к температуре (К) соответствовало этому отношению для аргона с множителем, равным кубу отношений атомных радиусов. Если, например, атомный радиус ксенона 0,218 нм, а радиус аргона 0,192 нм, то отношение давления к температуре для ксенона должно быть в (218/192)3 раз меньше, чем для аргона. При таком подборе температур отношения концентраций молекул в конденсированном состоянии и в состоянии пара были для разных веществ одинаковыми.
| Вещество | Неон | Аргон | Криптон | Ксенон | Свинец | Медь |
| Атомный Радиус нм. | 0,16 | 0,192 | 0,198 | 0,218 | 0,175 | 0,128 |
| Температура | 10,4 | 38,7 | ||||
| Теплота перехода. | ||||||
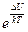
| 9,8×108 | 6×108 | 5,7×108 | 8,31×108 | 8,8×108 | 11×108 |
Для всех веществ, как видно из таблицы, получаются примерно одинаковые величины около 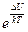 = 109. В рассматриваемом случае объемы вещества в состоянии пара и в конденсированном состоянии отличаются в 946 раз (примерно в 103). Средние расстояния между центрами молекул при переходе изменились примерно в 10 раз.
= 109. В рассматриваемом случае объемы вещества в состоянии пара и в конденсированном состоянии отличаются в 946 раз (примерно в 103). Средние расстояния между центрами молекул при переходе изменились примерно в 10 раз.
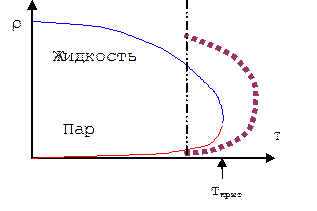
Если в конденсированном состоянии каждая молекула могла «свободно» перемещаться в выделенном направлении только на расстояние порядка D/100, то для «свободного» движения её центра масс предоставлялся объем, равный примерно D3×10-6. В состоянии пара для «свободного» движения центра масс молекулы предоставляется объём D3×103. Отношение этих объемов как раз соответствуют вычисленной величине 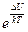 . Таким образом, отношение концентраций молекул, вычисленных с учетом объёма, предоставляемого для «свободного» движения центра масс молекулы, относятся именно так, как это предсказывает соотношение Больцмана. Из этого следует любопытный вывод: жидкость и пар – это одно и то же состояние. При одинаковой температуре они отличаются только отношением: внешнее давление/внутреннее давление!!! Кстати, этот вывод вовсе не является неожиданным. Для любого вещества возможен переход от газообразного состояния к жидкому состоянию с непрерывной сменой состояний и плавным изменением плотности. При таком переходе нет скачков плотности в пространстве и, соответственно, нет резкого перехода пар – жидкость. Осуществляется такая последовательность состояний в обход критической точки. На приведенном рисунке такой обход показан жирной пунктирной линией.
. Таким образом, отношение концентраций молекул, вычисленных с учетом объёма, предоставляемого для «свободного» движения центра масс молекулы, относятся именно так, как это предсказывает соотношение Больцмана. Из этого следует любопытный вывод: жидкость и пар – это одно и то же состояние. При одинаковой температуре они отличаются только отношением: внешнее давление/внутреннее давление!!! Кстати, этот вывод вовсе не является неожиданным. Для любого вещества возможен переход от газообразного состояния к жидкому состоянию с непрерывной сменой состояний и плавным изменением плотности. При таком переходе нет скачков плотности в пространстве и, соответственно, нет резкого перехода пар – жидкость. Осуществляется такая последовательность состояний в обход критической точки. На приведенном рисунке такой обход показан жирной пунктирной линией.
Дополнение:
| <== предыдущая страница | | | следующая страница ==> |
| Модели, описывающие состояние реальных веществ | | | Критическое состояние вещества |
Дата добавления: 2014-11-20; просмотров: 771; Нарушение авторских прав

Мы поможем в написании ваших работ!