
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Классификация методов осадительного титрования
Методы осадительного титрования классифицируют по типу титранта:
Ag(NO3) – аргентометрия;
Hg2(NO3)2 – меркурометрия;
Hg(NO3)2 – меркуриметрия;
H2SO4 – сульфатометрия;
BaCl2 – бариметрия и т.д.
Кривые осадительного титрования
Зависимость рI- = [I-]-изменение концентрации ионов в процессе титрования от объема добавленного титранта. Сравним кривые титрования 0,1 н растворов KCl, KBr, KI 0,1 н раствором нитрата серебра:
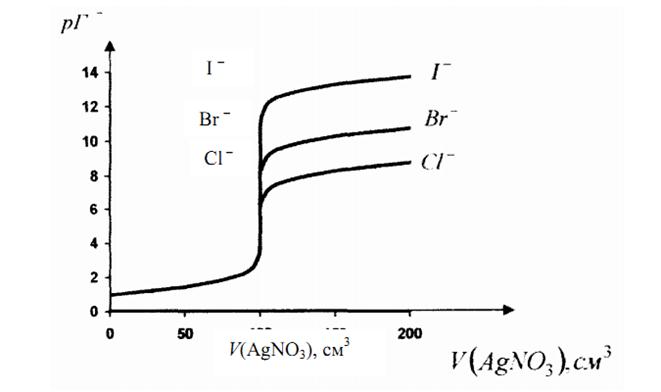
Анализ кривой титрования:
1. Кривая симметрична относительно точки эквивалентности.
2. Скачок титрования (3,8 – 6,2). Он зависит от:
– концентрации реагентов: чем меньше концентрация, тем меньше скачок титрования;
– растворимости осадка: чем меньше растворимость, тем больше скачок(у AgI больше, чем AgCl );
Применение метода
Аргентометрия – стандартный раствор AgNO3 . Метод используют в анализе фармпрепаратов – KI , KBr , NaI , NaBr , NaCl , спиртовых растворов I2, галогенсодержащих органических веществ, в основном для колличественного определения галоген-ионов и т.д. При этом образуются малорастворимые соли серебра.
В основе метода меркуриметрии– реакция образования малорастворимого Hg2Cl2 Индикатор – дифенилкарбазон, образующий с [Hg2]2+ осадок синего цвета.
Меркуриметрия и меркурометрия применяются для определения галогенидов, цианидов и ионов окисной ртути, но достаточно редко вследствие ядовитости солей ртути (I) и (II).
| <== предыдущая страница | | | следующая страница ==> |
| Лекция № 6 Осадительное титрование | | | Понятие механизма административно – правового регулирования |
Дата добавления: 2014-04-30; просмотров: 959; Нарушение авторских прав

Мы поможем в написании ваших работ!