
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ЭЛЕКТРОДНЫЕ ПОТЕНЦИАЛЫ И ЭЛЕКТРОДВИЖУЩИЕ СИЛЫ
14.1. Если металлическую пластинку опустить в воду, то катионы металла на её поверхности гидратируются полярными молекулами воды и переходят в жидкость. При этом электроны, в избытке остающиеся в металле, заряжают его поверхностный слой отрицательно. Возникает электростатическое притяжение между перешедшими в жидкость гидратированными катионами и поверхностью металла. В результате этого в системе устанавливается подвижное равновесие:
Me+MH2O→Me(H2O)nm+nē
в растворе на металле
где n – число электронов принимающих участие в процессе. На границе металл – жидкость возникает двойной электрический слой, характеризующийся определенным скачком потенциала. Абсолютные значения электронных потенциалов измерить не удается. Электродные потенциалы зависят от ряда факторов(природы металла, концентрации, температуры и др.). Поэтому обычно определяют относительные электродные потенциалы в определенных условиях – так называемые стандартные электродные потенциалы.(E0 ).
Стандартным электродным потенциалом у металла называют его электродный потенциал, возникающий при погружении металла в раствор собственного иона с концентрацией (или активностью), равное 1 моль/л, измеренный по сравнению со стандартным водородным электродом потенциал которого при 25º C условно принимается равным нулю ( E0=0; ∆G0=0).
Располагая металлы по мере возрастания их стандартных электродных потенциалов (Е0), получаем так называемый ряд напряжений.
Положение того или иного металла в ряду напряжений характеризует его восстановительную способность, а также окислительные свойства его ионов в водных растворах при стандартных условиях. Чем меньше значение E0, тем большими восстановительными способностями обладает данный металл в виде простого вещества и тем меньше окислительные способности проявляют его ионы, и наоборот. Электродные потенциалы измеряют в приборах, которые получили название гальванических элементов. Окислительно-восстановительная реакция, которая характеризует работу гальванического элемента, протекает в направлении, в котором ЭДС элемента имеет положительное значение. В этом случае ∆G0<0, так как ∆G0= -nFE0.
14.2. Примеры решения задач.
Пример 1. Стандартный электродный потенциал никеля больше, чем кобальта (табл.14.1). Изменится ли это соотношение, если измерить потенциал никеля в растворе его ионов с концентрацией 0,001 моль/л, а потенциалы кобальта – в растворе с концентрацией 0,1 моль/л.
Таблица 14.1Стандартные электродные потенциалы (E0) некоторых металлов (ряд напряжений).
| Электрод | E0, В | Электрод | E0, В |
| Li+/Li | -3,045 | Cd2+/Cd | -0,403 |
| Rb+/Rb | -2,925 | Co2+/Co | -0,277 |
| K+/K | -2,924 | Ni2+/Ni | -0,25 |
| Cs+/Cs | -2,923 | Sn2+/Sn | -0,136 |
| Ba2+/Ba | -2,90 | Pb2+/Pb | -0,127 |
| Ca2+/Ca | -2,87 | Fe3+/Fe | -0,037 |
| Na+/Na | -2,714 | 2H+/H2 | -0,000 |
| Mg2+/Mg | -2,37 | Sb3+/Sb | +0,20 |
| Al3+/Al | -1,70 | Bi3+/Bi | +0,215 |
| Ti2+/Ti | -1,603 | Cu2+/Cu | +0,34 |
| Zr4+/Zr | -1,58 | Cu+/Cu | +0,52 |
| Mn2+/Mn | -1,18 | Hg22/2Hg | +0,79 |
| V2+/V | -1,18 | Ag+/Ag | +0,80 |
| Cr2+/Cr | -0,913 | Hg2+/Hg | +0,85 |
| Zn2+/Zn | -0,763 | Pt2+/Pt | +1,19 |
| Cr3+/Cr | -0,74 | Au3+/Au | +1,50 |
| Fe2+/Fe | -0,44 | Au+/Au | +1,70 |
Решение. Электродный потенциал металла (E) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
E=E0+ 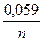 lgC,
lgC,
где E0 – стандартный электродный потенциал;
n – число электронов, принимающих участие в процессе;
C – концентрация (при точных вычислениях – активность) гидратированных ионов металла в растворе, моль/n;
E0 для никеля и кобальта соответственно равны – 0,25 и – 0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
ENi2+/Ni= -0,25 + 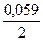 lg10-3= - 0,339 В,
lg10-3= - 0,339 В,
ECo2+/Co= - 0,277+ 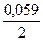 lg10-1= - 0,307 В.
lg10-1= - 0,307 В.
Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Пример 2. Магниевую пластинку опустили в раствор его соли. При этом электродный потенциал магния оказался равен – 2,41 В. Вычислите концентрацию ионов магния (в моль/л).
Решение. Подобные задачи решаются также на основании уравнения Нернста (см. пример 1):
- 2,41= - 2,37+ 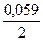 lgC,
lgC,
- 0,04=0,0295lgC,
lgC= - 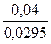 = - 1,3559= 2,6441,
= - 1,3559= 2,6441,
CMg2+=4,4∙10-2 моль/л.
Пример 3. Составьте схему гальванического элемента, в котором электродами являются магниевая и цинковая пластинки, опущенные в растворы их ионов с активной концентрацией 1 моль/л. Какой металл является анодом, какой катодом? Напишите уравнения Окислительно-восстановительной реакции, протекающей в этом гальваническом элементе, и вычислите его ЭДС.
Решение. Схема данного гальванического элемента:
( - )Mg│Mg2+││Zn2+│Zn (+)
Вертикальная линейка обозначает поверхность раздела между металлом и раствором, а две линейки – границу раздела двух жидких фаз – пористую перегородку (или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,37 В) и является анодом, на котором протекает окислительный процесс
Mg0 – 2e=Mg2+ (1)
Цинк, потенциал которого -0,763 В, - катод, т.е. электрод, на котором протекает восстановительный процесс:
Zn2++2e= Zn0, (2)
Уравнение окислительно-восстановительной реакции, характеризующие работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:
Mg+Zn2+=Mg2++Zn
Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода. Так как концентрация ионов в растворе равна 1 моль/л, то ЭДС элемента равна разности стандартных потенциалов двух его электродов:
ЭДС= E0 Zn2+/Zn – E0 Mg2+/Mg= - 0,763-(-2,37)=1,607 В.
14.3.Задания для контрольной работы.
261. В два сосуда с голубым раствором медного купороса поместили в первый цинковую пластинку, а во второй серебряную. В каком сосуде цвет раствора постепенно пропадет? Почему? Составьте электронные и молекулярные уравнения соответствующей реакции.
262. Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: а) CuSO4; б) MgSO4; в) Pb(NO3)2? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
263. При какой концентрации Zn2+ (в моль/л) потенциал цинкового электрода будет на 0,015В меньше его стандартного электродного потенциала? Ответ: 0,30 моль/л.
264. Увеличится, уменьшится или останется без изменения масса кадмиевой пластинки при взаимодействии ее с растворами: а) AgNO3; б) ZnSO4; в) NiSO4? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
265. Марганцевый электрод в растворе его соли имеет потенциал -1,23В. Вычислите концентрацию ионов Mn2+(в моль/л). Ответ: 1,89∙10-2 моль/л.
266. Потенциал серебряного электрода в растворе AgNO3 составил 95% от значения его стандартного электродного потенциала. Чему равна концентрация ионов Ag+ (в моль/л)? Ответ:0,20 моль/л.
267. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС медно- кадмиевого гальванического элемента, в котором [Cd2+]=0,8 моль/л, а [Cu2+]=0,01 моль/л. Ответ: 0,68 В.
268. Составьте схемы двух гальванических элементов, в одном из которых медь была бы катодом, в другом – анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и аноде.
269. При какой концентрации ионов Сu2+ (моль/л) значение потенциала медного электрода становится равным стандартному потенциалу водородного электрода? Ответ: 1,89∙10-12 моль/л.
270. Какой гальванический элемент называется концентрационным? Составьте схему, напишите электродные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из серебряных электродов, опущенных: первый в 0,01 н, а второй – в 0,1 н растворы AgNO3. Ответ: 0,059 В.
271. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один никелевый электрод находится в 0,001 М растворе, а другой такой же электрод – в 0,01 М растворе сульфата никеля. Ответ: 0,0295 В.
272. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин. 
щенных в растворы своих солей с концентрацией [Pb2+] = [Mo2+] = 0,01 моль/л. Изменится ли ЭДС этого элемента, если концентрацию каждого их ионов увеличить в одинаковое число раз? Ответ: 2,244 VH 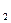 В.
В.
273. Составьте схемы двух гальванических элементов, в одном из которых никель является катодом, а в другом – анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и на аноде.
274. Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на аноде и на катоде.
275. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего их пластин кадмия и магния, опущенных в растворы своих солей с концентрацией [Mg2+] = [Cd2+] = 1моль/л. Изменится ли значение ЭДС, если концентрацию каждого их ионов понизить до 0,01моль/л. Ответ: 1,967В.
276. Составьте схему гальванического элемента, состоящего из пластин цинка и железа, погруженных в растворы их солей. Напишите электронные уравнения процессов, протекающих на аноде и на катоде. Какой концентрации надо было взять ионы железа (моль/л), чтобы ЭДС элемента стала равна нулю, если [Zn2+] = 0,001моль/л. Ответ: 7.3 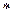 10-15моль/л.
10-15моль/л.
277. Составьте схему гальванического элемента, в основе которого лежит реакция, протекающая по уравнению:
Ni + Pb(NO3)2 = Ni(NO3)2 + Pb
Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элемента, если [Ni2+] = 0,01моль/л, а [Pb2+] = 0,0001моль/л. Ответ: 0,064В.
278. Какие химические процессы протекают на электродах при зарядке свинцового аккумулятора?
279. Какие химические процессы протекают на электродах при зарядке и разрядке кадмий-никелевого аккумулятора?
280. Какие химические процессы протекают на электродах при зарядке и разрядке железо-никелевого аккумулятора?
| <== предыдущая страница | | | следующая страница ==> |
| Хлор и ок-ль и восст-ль | | | ЭЛЕКТРОЛИЗ. 15.1.Электролизом называется совокупность окислительно-восстановительных процессов, которые протекают при пропускании постоянного электрического тока через |
Дата добавления: 2014-09-08; просмотров: 1221; Нарушение авторских прав

Мы поможем в написании ваших работ!