
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Производство глутаминовой кислоты и глутамата натрия
Таблица 1 - Потребность человека в незаменимых аминокислотах
| Аминокислоты | Потребность, мг/кг массы тела в сутки | |
| младенцы | взрослые | |
| валин | ||
| гистидин | ||
| изолейцин | ||
| лейцин | ||
| лизин | ||
| метионин (и цистеин) | ||
| фенилаланин (и тирозин) | ||
| треонин | ||
| триптофан |
В промышленных масштабах белковые аминокислоты получают:
- гидролизом природного белоксодержащего сырья;
- химическим синтезом;
- микробиологическим синтезом;
- биотрансформацией предшественников аминокислот с помощью микроорганизмов или ферментов (химико-микробиологический метод).
При гидролизебелоксодержащее сырье (отходы пищевой и молочной промышленности) нагревают с растворами кислот или щелочей при температуре 100 - 105 0С в течение 20 - 48 ч. Чаще всего используют 20 % раствор соляной кислоты, обеспечивающий глубокий гидролиз белка. В ходе кислотного гидролиза белков происходят рацемизация и разрушение некоторых составляющих их аминокислот. При кислотном гидролизе полностью разрушается триптофан и достаточно значительны потери цистеина, метионина и тирозина (10 - 30 %). Лучшим способом уменьшения потерь аминокислот при гидролизе является проведение его в вакууме или в атмосфере инертного газа.
Существенный недостаток методов химического синтезааминокислот состоит в получении целевых препаратов в виде рацемической смеси D- и L-стереоизомерных форм. Подавляющее большинство природных аминокислот относится к L-ряду. D-α-аминокислоты обнаружены лишь в составе гликопротеинов клеточных стенок бактерий, антибиотиков и некоторых токсинов. Проницаемость L-аминокислот в клетке в 500 раз превышает таковую ее антипода. Стереоспецифичны также транспорт и метаболизм аминокислот. Исключением в этом отношении является лишь метионин, метаболизм которого нестереоизбирателен, благодаря чему данная аминокислота получается преимущественно путем химического синтеза. Разделение рацематов других аминокислот - дорогая и чрезвычайно трудоемкая процедура. Наиболее перспективен и экономически выгоден микробиологический синтезаминокислот. Более 60 % всех производимых в настоящее время промышленностью высокоочищенных препаратов белковых аминокислот получают именно таким способом, главное преимущество его в сравнении с методами химического синтеза состоит в возможности получения L-аминокислот на основе возобновляемого сырья. В последние годы при производстве аминокислот все шире используют биотрансформацию предшественников аминокислот, особенно с помощью иммобилизованных ферментов или клеток микроорганизмов, предварительно получаемых химическим путем. Промышленное производство аминокислот стало возможным после открытия способности у некоторых микроорганизмов выделять в культуральную среду значительные количества какой-либо одной аминокислоты.
Таблица 2 - Микроорганизмы - продуценты аминокислот
| Продуценты аминокислот | Микроорганизмы |
| Агринин | Е. cоli. Bacillus subtilis, Corynebacterium glutamicum, Brevibacterium flavum, Serratia marcescens |
| Гистидин | B.flavum, C. glutamicum, S.marcescens, виды Steptomyces |
| Изолейцин | B.flavum, С glutamicum, B. subtilis, S. marcescens |
| Лейцин | Brevibacterium lactofermentum, S. marcescens, C. glutamicum |
| Лизин | B. flavum, С. glutamicum |
| Фенилаланин | B. flavum, С. glutamicum |
| Пролин | B. flavum |
| Серин | С. glutamicum |
| Треонин | В. flavum, С. Glutamicum, Arthrobacter parafinens, E. coli S. marcescens |
| Триптофан | Micrococcus, Candida utils, B. subtilis |
| Тирозин | B. flavum, С. glutamicum |
| Валин | B. flavum, С. glutamicum |
В России изыскания в области промышленного синтеза аминокислот были начаты в 50-х годах прошлого столетия по инициативе академика А.А. Александрова. Перспективные штаммы продуцентов постоянно улучшают посредством селекции мутантов с измененной генетической программой и регуляторными свойствами. Распространенные объекты селекции продуцентов - микроорганизмы, относящиеся к Brevibacterium, Micrococcus, Corynebacterium, Arthrobacter (таблица 2).
Биотехнология производства аминокислот
L-глутаминовая кислота (a-аминоглутаровая) – первая аминокислота, полученная на основе промышленного микробиологического синтеза:
НООС – СН2 – СН2 – NH2СН – СООН
Глутаминовая кислота является важнейшей аминокислотой растительных и животных белков, не будучи незаменимой. Синтез глутаминовой кислоты происходит в цикле трикарбоновых кислот (рисунок 31) в результате ферментативного восстановительного аминирования 2-кетоглутаровой кислоты НАДФ-зависимой глутаматдегидрогеназой:
НООС – СН2 – СН2 – СО– СООН + НАД(Ф)Н2 + NН3 ®
® НООС – СН2 – СН2 – NН2СН – СООН + НАД(Ф).
Возможность получения глутаминовой кислоты из углеводов на основе микроорганизмов впервые была продемонстрирована в 1957 г. японскими исследователями Киносита, Асаи и др. Продуцировать глутаминовую кислоту способны дрожжи, микроскопические грибы, бактерии. Бактерии обеспечивают наибольший выход по отношению к использованному углеродному субстрату (не менее 40–50 %). Промышленное значение имеют бактериальные культуры (Micrococcus, Brevibacterium, Microbacterium, Corynebacterium). Сверхсинтез кислоты у диких штаммов возможен в специальных физиологических условиях при торможении скорости роста и увеличении проницаемости клеточной мембраны для глутаминовой кислоты.Глутаминовая кислота в основном используется в фармакологии и пищевой промышленности, поэтому задача постферментационной стадии – получение высокоочищенных препаратов. Для этого на первом этапе обработки культуральной жидкости в нее добавляют негашеную известь или известковое молоко. После этого избыток ионов осаждают кислотой, осадок удаляют центрифугированием. Фильтрат после осветления активированным углем и сорбции на ионообменных смолах концентрируют вакуум-выпариванием при 40 - 60°С. Осаждение кристаллов глутаминовой кислоты проводят в изоэлектрической точке (рН 3,2 при 4 - 15°С). В результате перекристаллизации чистота продукта достигает 99,6 %.
Кристаллы кислоты отделяют от маточника центрифугированием, промывают и высушивают. Если нужно получить глутамат натрия, кристаллы глутаминовой кислоты обрабатывают гидроокисью натрия. Для этого влажные кристаллы растворяют в воде, нейтрализуют 50 % раствором едкого натра. Полученный раствор фильтруют, упаривают под вакуумом до содержания сухих веществ 60% и направляют на перекристаллизацию. Полученные кристаллы глутамата натрия выделяют из маточного раствора центрифугированием и высушивают током горячего воздуха. Глутамат натрия усиливает вкус многих пищевых продуктов, способствует длительному сохранению вкусовых качеств консервированных продуктов (овощей, рыбы, мясных продуктов). Важное свойство глутаминовой кислоты – служить защитным фактором при отравлениях внутренних органов, ослаблять действие токсинов и усиливать ряд фармакологических препаратов. В настоящее время производство глутаминовой кислоты является крупнотоннажным биотехнологическим производством (около 400 тыс. т/г).
Получение лизина и триптофана
Процесс получения лизина основан на стереоспецифическом ферментативном гидролизе (конверсии) D-,L-a-амино-е-капролактама, который сначала получают химическим путем из циклогексена:
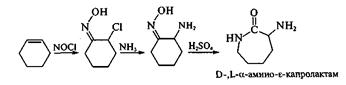
Рацемат используют в качестве субстрата, который под действием фермента L-а-амино-е-капролактамгидролазы (лактамаза) превращается в L-лизин, а оставшаяся непрореагировавшая его часть (β-форма) переводится при воздействии рацемазы в смесь антиподов:
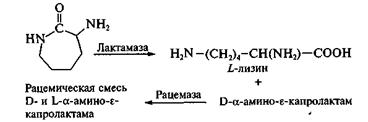
Лактамаза найдена у некоторых видов дрожжей, в частности - у Candida laurentii. У них синтез фермента индуцируется добавлением субстрата (рацемической смеси), а активность энзима поддерживается при добавлении в среду ионов Мg2+, Мn2+.
Рацемаза обнаружена у ряда бактерий. Для получения неочищенных ферментов целые клетки микроорганизмов обрабатывают поверхностно-активными веществами, вызывающими изменение проницаемости стенки клеток микроорганизмов-продуцентов. Разработаны иммобилизованные формы обоих ферментов. При производстве лизина в водный раствор D-,L-a-амино-е-капролактама одновременно вводят источники лактамазы и рацемазы, содержащиеся в дрожжевых и бактериальных клетках. Процесс осуществляется при температуре 30-50°С, рН 8,0-8,5 и оптимальном режиме аэрации. На выходе из реактора образуется преимущественно один продукт - лизин, который выделяют из смеси, очищают и сушат. Описанная технология получения лизина, распространенная в США и Японии, по завершении процесса обеспечивает содержание аминокислоты в реакционной среде свыше 150 г/л.

Рисунок 1 - Диаминопимелиновый путь синтеза лизина
Получение триптофана
Химико-ферментативный способ получения триптофана состоит в прямой конденсации индола, аммиака и пировиноградной кислоты:
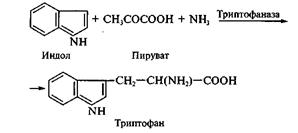
Реакцию катализирует пиридоксальзависимая триптофан-индоллиаза (триптофаназа). Фермент широко распространен в природе. Он найден у бактерий Е. соli и характеризуется широкой субстратной специфичностью. Кроме L-триптофана его субстратами служат L-цистеин, 8-метил-цистеин, хлор-L-аланин, L-серин. Добавление триптофана индуцирует образование фермента, а добавление индола ингибирует его синтез у бактерий, поэтому процесс получения триптофана ведут при избытке аммиака и пирувата.
Выход аминокислоты при реализации химико-энзиматического способа получения триптофана составляет 63 г/л. Подобно лизину триптофан образуется в ходе разветвленного метаболического пути, поэтому для его производства используют ауксотрофные мутанты, у которых блокированы реакции, ведущие к синтезу фенилаланина и тирозина. Наряду с другими ароматическими аминокислотами у микроорганизмов (подобно большинству организмов) триптофан образуется из метаболитов углеводного обмена - эритрозо-4-фосфата и фосфоенолпирувата. Метаболическим предшественником триптофана служит антраниловая кислота, возникающая из хоризмовой кислоты под действием антранилат-синтетазы. Триптофан оказывает ингибирующее действие на антранилатсинтетазу, поэтому для обхода метаболического контроля синтез фермента индуцируют ступенчатым введением предшественника - антраниловой кислоты (0,1 - 0,3 %):
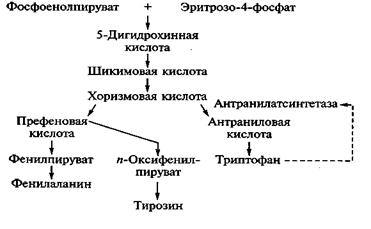
В связи с этой особенностью промышленное производство триптофана организовано преимущественно по двухступенчатой схеме. На первом этапе химическим способом синтезируют антраниловую кислоту, которую с помощью энзиматической системы мутантных штаммов дрожжей Саndida utilis переводят в триптофан. Биомассу дрожжей выращивают при температуре 30°С в среде, содержащей свекловичную мелассу, мочевину и минеральные компоненты. Через сутки в ферментер вводят 5 % спиртовой раствор антраниловой кислоты и 50 % раствор мочевины, а через 3 - 4 ч. после введения предшественника дополнительно добавляют источник углерода (25 % раствор мелассы). Антраниловую кислоту и мочевину подают через каждые 6 ч, а мелассу - через каждые 12 ч. Процесс двухступенчатой ферментации завершается через 144 ч. и обеспечивает содержание триптофана в культуральной среде до 6 г/л. Кроме триптофана, микробиологическим способом с использованием предшественников получают гистидин, изолейцин, метионин, серин и треонин. Менее распространены одноступенчатые технологии получения триптофана на основе ауксотрофных мутантов бактерии Bacilius subtilis,осуществляемые по схеме, близкой к способу получения лизина. Длительность одноступенчатого процесса - 48 ч, а концентрация триптофана в культуральной среде составляет 10 г/л. После сушки культуральной жидкости получают кормовой концентрат триптофана (ККТ), который включает белки, свободный триптофан, витамины В1, В2 и РР. Высокоочищенные кристаллические препараты триптофана образуются после дополнительной очистки культуральной жидкости методом ионообменной хроматографии на колонке, заполненной катионитом (сорбция при рН 1,0; элюция 5% раствором гидроксида аммония в смеси с пропанолом). Элюаты кристаллизуют; кристаллы отмывают и высушивают. Кристаллический препарат содержит до 99 % триптофана.
Лекция 12. Получение биологически активных добавок (БАД). Фототрофные микроорганизмы - продуценты биологически активных добавок к пище. Применение БАД в пищевой промышленности.
БАД (биологически активные добавки к пище) - термин, вошедший в современную медицину сравнительно недавно. Однако ещё до новой эры в Египте, Китае, Тибете, Индии и других странах Востока сложились довольно стройные системы профилактики и терапии различных заболеваний человека путём использования чаще всего в натуральном виде специально приготовленных продуктов из растительных, животных тканей, минерального сырья. История начала производства специальных фармакологических форм для лечения болезней человека относится примерно к 130-200 г. н.э., когда К. Галеном впервые были разработаны технологические приёмы изготовления лекарств (настоев, экстрактов, порошков) из природного сырья. Однако выдающиеся достижения химии конца XIX и XX веков, особенно в области органического синтеза, позволили получать настолько высокоэффективные лекарственные средства, что многие учёные-медики стали отказываться от прежних фитотерапевтических средств.
Казалось, что неограниченные возможности органической химии в получении чистых химических соединений с известной структурой и заданными свойствами, их высокая эффективность и возможность точного дозирования, узкая направленность действия - вот те достаточно убедительные аргументы, которые до недавнего времени не позволяли делать сколько-нибудь оптимистических прогнозов в области так называемой традиционной медицины. Однако такого рода взгляды оказались ошибочными.
Применение БАД в пищевой промышленности.
Последние годы характеризуются бурным развитием новой, пограничной между наукой о питании и фармакологией области знаний - фармаконутициологии.
Выдающийся отечественный учёный А.А. Покровский в своей книге «Метаболические аспекты фармакологии и токсикологии пищи» отмечал, что «пища - определение гораздо более ёмкое, чем это принято представлять. Это комплекс многих сотен тысяч (и, может быть миллионов) веществ, каждое из которых обладает определённой мерой биологической активности. Многие из биологически активных веществ обнаруживаются в продуктах питания в равных, а иногда и более высоких дозах, чем они используются в фармакологии. Пищу следует рассматривать не только как источник энергии и пластических веществ, но как весьма сложный фармакологический комплекс».
В динамике изменения структуры питания человека в историческом аспекте можно чётко выделить следующие общие для населения всех индустриально развитых стран явно неблагоприятные тенденции, сложившиеся к настоящему времени:
- избыточное потребление жиров животного происхождения (насыщенных жирных кислот), богатых холестерином;
- значительное увеличение потребления сахара и соли;
- существенное уменьшение потребления крахмала и пищевых волокон (в частности, клетчатки);
- выраженный круглогодичный дефицит в рационах витаминов, микроэлементов, биологически активных веществ различной природы.
Особую тревогу в последние годы вызывает пищевой статус россиян, который в настоящее время характеризуется повсеместно выявляемым круглогодичным глубоким дефицитом как у взрослых, так и у детей, большинства витаминов, в том числе витаминов антиоксидантного ряда - С. Е, А и бета-каротина. Выявляется существенный дефицит кальция, железа, йода, фтора, даже в питании детей, беременных и кормящих женщин.
Последствия выявленных нарушений структуры питания для здоровья населения:
- прогрессирующее увеличение в последние годы числа взрослых со сниженной массой тела и детей раннего возраста со сниженными антропометрическими показателями (12-14%);
- широкое распространение среди взрослых различных форм ожирения (среди лиц старше 30 лет избыточная масса тела и ожирение выявляются у 55%);
- частое выявление среди населения лиц с нарушенным иммунным статусом, в частности с различными формами иммунодефицитов, со сниженной резистентностью к инфекциям и другим факторам окружающей среды;
- увеличение частоты таких алиментарно-зависимых заболеваний, как железодефицитные анемии у взрослых и детей, связанные с дефицитом йода нарушения функции и заболевания щитовидной железы, а с дефицитом кальция заболевания опорно-двигательного аппарата и др.
БАД - это не лекарства, это природные или идентичные природным биологически активные вещества, получаемые из растительного, животного или минерального сырья.
Использование БАД к пище в повседневном питании больных и здоровых людей позволяет:
- достаточно легко и быстро восполнить дефицит эссенциальных (незаменимых) пищевых веществ, в первую очередь, микронутриентов;
- в определенной степени направленно изменять метаболизм отдельных веществ, в частности токсикантов;
- повысить неспецифическую резистентность организма к воздействию неблагоприятных факторов окружающей среды;
- получить механизм немедикаментозного, безопасного пути регулирования и поддержки функции отдельных органов и систем организма человека, обеспечивая тем самым повышение уровня здоровья, снижение заболеваемости, продление жизни человека.
БАД к пище можно подразделить на:
- Нутрицевтики;
- Парафармацевтики.
Нутрицевтики - незаменимые пищевые вещества или их близкие предшественники (например, бета-каротин и другие каратиноиды, омега-3 и другие полиненасыщенные жирные кислоты, некоторые микроэлементы - селен, железо, фтор, цинк, йод, макроэлементы - кальций и магний, отдельные незаменимые аминокислоты и их комплексы, некоторые моно- и дисахариды,. пищевые волокна и т. д.)
Использование нутрицевтиков позволяет:
- Достаточно легко и быстро ликвидировать дефицит эссенциальных пищевых веществ, повсеместно обнаруживаемый у большинства взрослого и детского населения России;
- Максимально индивидуализировать питание конкретного здорового человека в зависимости от потребностей, существенно отличающихся не только по полу, возрасту, интенсивности физической нагрузки, но и в связи с генетически обусловленными особенностями биохимической конституции отдельного индивидуума, его биоритмами , физиологическим состоянием (беременность, лактация, эмоциональный стресс и т. п.), а также экологическими условиями зоны обитания;
- Максимально удовлетворять изменённые физиологические потребности в пищевых веществах больного человека, а также (по принципу метаболического шунтирования) обойти повреждённое звено метаболического конвейера;
- Повысить за счёт усиления элементов ферментной защиты клетки неспецифическую резистентность организма к воздействию неблагоприятных факторов окружающей среды у населения, проживающих в экологически неблагополучных регионах;
- Усилить и ускорить связывание и выведение чужеродных и токсичных веществ из организма;
- Направленно изменять путём воздействия, прежде всего, на ферментные системы метаболизма ксенобиотиков, метаболизм отдельных веществ, в частности токсикантов.
Иными словами, применение БАД-нутрицевтиков является эффективной формой первичной и вторичной профилактики, а также комплексного, вспомогательного лечения больных при таких широко распространенных заболеваниях, как ожирение, атеросклероз и другие сердечно-сосудистые заболевания, злокачественные новообразования , иммунодефицитные состояния.
Парафармацевтики- это, как правило, продукты, содержащие органические кислоты, биофлавоноиды, дубильные, фенольные соединения, гликозиды, кофеин, биогенные амины, органические кислоты и другие так называемые натуропродукты. Их действие направлено на активацию и стимуляцию функции отдельных органов и систем в пределах физиологических границ (например, стимуляция секреторной, моторно-эвакуаторной функции кишечника пищевыми волокнами, стимуляция, умственной и физической работоспособности адаптогенами, регуляция липидно-олестеринового обмена, функции ЦНС, сердечно-сосудистой системы и т. д.)
Парафармацевтики не относятся к лекарствам и не могут их заменить!
Основные отличия парафармацевтиков от лекарств:
- Количество действующего начала в суточной дозе не должно превышать разовую терапевтическую дозу этого вещества в случае, если оно применяется в химически чистом виде в качестве лекарственного средства;
- Применяются парафармацевтики исключительно внутрь;
- Количественные изменения параметров функционирования систем и органов организма при применении парафармацевтиков лежат в пределах их физиологической нормы;
- Широкий диапазон используемых доз, при которых парафармацевтики оказывают своё нормализующее или корректирующее действие на функции при существенно более низкой вероятности проявления, по сравнению с лекарственными средствами, токсических и побочных эффектов.
При применении парафармацевтиков не исключены и явления индивидуальной непереносимости пациентом отдельных их компонентов, что характерно и для некоторых пищевых продуктов и ещё более для лекарственных средств. Эти явления чаще могут наблюдаться у людей с различными хроническими заболеваниями.
Лекция 13. Современная пищевая биотехнология. Использование пищевых добавок. Консерванты, ароматизаторы, красители, компоненты пищевых добавок. Генетически модифицированные продукты. Гигиеническая систематика пищевых добавок.
Современная пищевая биотехнология
Биотехнология- это одна из перспективнейших и бурноразвивающихся отраслей промышленности. Основные направления биотехнологии - пищевая, фармакологическая, медицинская, сельскохозяйственная биотехнологии. Современная биотехнология - это экологически чистые производства лекарственных препаратов, биосинтез белков, аминокислот, витаминов, ферментов и сверхактивных гормонов для сельского хозяйства и медицины, а также создание пищевых и вкусовых веществ.
Издревле человечество использует для своих нужд различные белковые вещества и биологически-активные соединения. К ним относятся белки, аминокислоты, углеводы, липиды, витамины и т. п. Все они сосредоточены в продуктах используемых в пищу. Следовательно, это специализация тесно связана с технологией производства пищевых продуктов. Сейчас пищевая промышленность превратилась в мощную отрасль народного хозяйства. Использование классических и внедрение новых технологий производства пищи, внедрение в строй современных производств по выработке новых продуктов питания, вкусовых добавок диктует необходимость подготовки высококвалифицированных специалистов в этой области. Вместе с тем пищевая промышленность требует коренной реконструкции и модернизации, в которой важную роль играет биотехнология и следовательно инженеры-биотехнологи.
Использование пищевых добавок. Консерванты, ароматизаторы, красители, компоненты пищевых добавок.
Пигменты. Основные потребности промышленности в этих соединениях удовлетворяются за счет природных источников и химического синтеза, но два из них, β-каротин и рибофлавин, традиционно получают методами биотехнологии. Последний образуется при глубинном культивировании Eremothecium ashbyii или Ashbya gossypii. Возможности микробиологического производства нетоксичных пищевых красителей исчерпаны далеко не полностью β-каротина сегодня вырабатывают очень мало, а важную группу красителей красного цвета до сих пор получают из виноградных выжимок (экстракта).
Подкислители .Подкислители применяются в основном как вкусовые добавки для придания продуктам острого вкуса. В практику они вошли скорее всего в результате широкого использования органических кислот для сохранения пищи. По-видимому, самым популярным подкислителем в пищевой:
промышленности сегодня является лимонная кислота. Сначала этот важный продукт получали, отжимая сок из лимонов. (в Италии): таким путем до начала 20-х годов удовлетворялось три четверти мировой потребности в лимонной кислоте. Сегодня ее получают при участии А. niger сбраживая мелассу и содержащие глюкозу гидролизаты. Отметим, что процесс сбраживания нужно строго контролировать, так как лимонная кислота в отличие от других вторичных метаболитов играет важную роль в регуляции обмена веществ. При консервировании помидоров широко используют яблочную кислоту; ее образует А. flavus.К числу других кислот, находящих широкое применение в пищевой промышленности, относятся итаконовая (продуцент — А.terreus), глюконовая, используемая в форме глюконолактона (продуцент — А.niger), и фумаровая (виды Rhizopus ).
Усилители вкуса. Расщепляя с помощью нуклеазы Реniсillит citrinum нуклеиновые кислоты, получают в промышленном масштабе 5-нуклеотиды (содержащие главным образом инозин и гуанин), которые выходят применение как усилители вкуса. Вещества, усиливающие оттенки вкуса, содержатся и в природных пищевых продуктах. Главным усилителем вкуса считается натриевая соль глутаминовой кислоты: ее можно получить при помощи Microccocus glutamicus. Пионером использования усилителей вкуса является Япония, но сам принцип применялся при создании рецептов многих блюд во всем мире.
Жиры и масла. Анализ перспектив использования жиров и масел, продуцируемых бактериями (в особенности содержащих необычные полиненасыщенные жирные кислоты, а потому дорогостоящих), показал, что в нынешних экономических условиях использовать эти вещества вместо жиров растительного и животного происхождения нецелесообразно.
Растительные клеи и загустители. Натуральные растительные клеи, получаемые из камедей растений или морских водорослей, принадлежат к числу давно известных пищевых добавок; в Китае, например, они широко употреблялись еще в первом столетии до нашей эры, а об их использовании упоминается даже в Ветхом завете. Растительные клеи относятся к группе пищевых добавок — гидроколлоидов. Их применяют для изменения консистенции пищевых продуктов: эти вещества способствуют их загущению и образованию студней. Структура пищевых продуктов при этом стабилизируется, улучшаются их внешний вид и вкус. Большое значение для этой отрасли имеет разработка промышленного производства полисахаридов из Pseudomonas spp. Их предполагается использовать вместо ,,глюкойаннозы, одного из наиболее широко применяемых загустителей. Свойства этого нового продукта детально изучены. В кондитерской промышленности и при производстве мороженого в качестве стабилизатора сегодня широко используется декстран из Leuconostoc mesenteroides.
Консервированные овощи. Как и в случае многих других разновидностей пищевого сырья, необходимость сохранения овощей для употребления их в течение всего года привела к созданию ряда новых пищевых продуктов. до того как в практику вошли консервирование в банках и замораживание, для сохранения овощей использовалась главным образом соль. Низкие концентрации соли (2—2,5%) при переработке содержащих сахара овощей с малой долей белков не препятствуют брожению с образованием кислот, идущему при участии бактерий. Этот способ дает хорошие результаты, но если белка в овощах много (горох, фасоль),то продукт портится. Если такие овощи засаливают, то соли добавляют столько, чтобы полностью подавить брожение. Когда соли добавляют мало, основную роль в консервации играют молочнокислые бактерии. Образование молочной кислоты из сахаров препятствует развитию бактерий кишечной группы, протеолитических бактерий, анаэробных и спорообразующих видов. Кислую капусту готовят из свежей измельченной капусты. После добавления соли на первых стадиях брожения доминируют бактерии Leuconostoc mesenteroides, которые в анаэробных условиях превращают сахара в молочную и уксусную кислоты,, этиловый спирт, маннитол, эфиры и СО2. В дальнейшем образование молочной кислоты из сахаров и маннитола осуществляется при участии Lactobacillus plontarum. Разложение маннитола — важный этап, так как он придает продукту горький вкус. Хотя при получении кислой капусты условия сбраживания в какой-то степени контролируются, применять закваски нет необходимости, так как никаких преимуществ они не дают.
Пикули делают из засоленных огурцов. Конечный продукт получают путем полного или частичного сбраживания либо без такой обработки. При брожении важную роль опять-таки играют молочнокислые бактерии, осуществляющие ферментацию сахаров. Соли обычно добавляют немного, и рассол с самого начала подкисляют уксусной кислотой. Если к нему добавляют укроп и другие пряности, то получают укропные пикули.Оливки перерабатывают путем засолки и обработки щелоком. Когда консервируют зеленые плоды, молочнокислое брожение осуществляется при участии Leuconostoc mesenteroides , а затем Lactobacillus plonarumи продолжается от шести до десяти месяцев. Спелые оливки либо не сбраживают вовсе, либо сбраживают недолго. И в том и в другом случае большое значение имеет обработка щелоком, так как при этом удаляется олеуропеин (глюкозид, имеющий горький вкус). Микроорганизмы играют важную роль и на определенных стадиях выработки некоторых других продуктов, особенно кофе и какао. При замочке плодов на них развиваются молочнокислые бактерии и дрожжи, что способствует отделению кожуры от зерен; влияние микробов на качество конечного продукта незначительно.Приведенные примеры использования микроорганизмов в переработке овощей — это процессы с простой технологией. Хотя в случае засолки деятельность микробов и определяет основные свойства конечного продукта, суть ее проста — это в основном образование кислотьт. Сходную продукцию можно получить за более короткое время — для этого достаточно добавить к свежим овощам соответствующие кислоты и тем самым обойтись без брожения. Отметим, что, хотя для сохранения овощей используются главным образом консервирование в банках и замораживание, спрос на заквашенные продукты сохраняется, так как они обладают специфическим вкусом.
Продукты из сои. Соя издавна принадлежит к числу главных пищевых культур в странах Азии, особенно в Китае и Японии. В восточной кухне она служила главным поставщиком белка и масла задолго до того, как ее стали использовать как источник этих веществ в странах Запада. На основе соевых бобов на Востоке вырабатывают множество традиционных пищевых продуктов; их особый вкус определяется деятельностью микроорганизмов. Это главным образом грибы, в частности представители рода Aspergillus. Соевый соус готовят на основе кашицы из набухших и отваренных бобов сои. В нее вносят закваску, содержащую разнообразные микроорганизмы, главным образом Аspergillus oryzae. В ходе Выдержки в течение 3 — 5 суток при 25 – 30 ºC гриб активно разрастается на поверхности. Затем в смесь добавляют соль (до 20%) и оставляют ее созревать на 0,5—2 года. В настоящее время применяют чистые культуры А. oryzae, поэтому срок выдержки сокращается до одного - трех месяцев. В завершение жидкость сливают с массы или отделяют под прессом и получают соевый соус. Помимо ускорения процесса путем использования чистых культур разработаны и сугубо химические способы получения соевых гидролизатов. Так готовят несброженный соевый соус.
В Японии из размельченных соевых бобов (иногда с добавкой риса делают похожую приправу — тамари. Продолжительность сбраживания при этом меньше, чем в случае китайского соевого соуса, а ведущую роль в процессе играет Аspergillus tamari. Еще одну приправу, мизо, готовят в Японии из отваренных соевых бобов, которые заражают А. oryzae, добавляют к ним соль и воду и ставят на созревание на несколько дней, после чего тщательно измельчают. Когда делают натто, сваренные соевые бобы укутывают в рисовую солому и ставят на созревание на 1—2 суток. Главную роль здесь играет Bacillus subtilis, образующая слизистую пленку. В Восточной кухне часто используется соевый сыр, или курд. Соевые бобы сначала замачивают и измельчают в пасту, а затем отжимают ее через полотно. для створаживания применяют соли кальция и магния и полученный продукт формуют в виде кубиков. В ходе выдержки в течение месяца при 14ºC активно развиваются белые плесневые грибы. Окончательное созревание происходит в рассоле или особым образом сделанном вине.
Современная биотехнология, видимо, лишь в малой степени может способствовать развитию этих традиционных производств. Все произошедшие здесь изменения заключались обычно в уменьшении времени ферментации; в отдельных случаях процессы стали безмикробными. Впрочем, возможно дальнейшее усовершенствование процессов путем улучшения штаммов и контроля за ферментацией. Кроме того, соевые бобы могут стать тем сырьем, из которого на основе традиций восточной кухни для рынка как Запада, так и Востока можно будет получать совсем новые продукты ферментации. В этих случаях перерабатываются целые бобы, однако известны уже и полученные с помощью биотехнологии новые продукты из белков сои. Их вырабатывают путем контролируемого гидролиза белков сои ‘ферментами микроорганизмов. Свойства таких продуктов (растворимость, вкус и т. д.) можно в определенной мере регулировать. Наиболее привлекательным из них представляется изо- электрический растворимый гидролизат белков сои. Как заменитель мяса он лучше, чем блюда из соевых бобов. В странах где население получает с пищей недостаточно белка, им обогащают безалкогольные напитки.
Применение ферментов при выработке фруктовых соков.
Применение ферментов из микроорганизмов — один из главных путей, которые биотехнология использует и будет использовать. для обновления пищевой промышленности. Наибольшие успехи были достигнуты при производстве фруктовых соков: здесь ис— пользуют такие ферменты, как пектиназы, целлюлазы, гемицеллюлазы, амилазы и протеиназы. Эти ферменты применяются не только в давно освоенных производствах; с их помощью удалось расширить ассортимент и добиться большего выхода продукции из сырья. Ферменты используются на следующих основных стадиях переработки фруктов.. Обработка мезги:разрушение мякоти при- выработке фруктовой кашицы или нектаров; увеличение выхода сока; лучшее отделение веществ, ответственных- за цвет и вкус. 2. Обработка сока: уменьшение вязкости; облегчение изготовления концентратов; упрощение процедур осветления, фильтрования и стабилизации сока.Выбор ферментов и способов их применения для получения наилучших результатов при выработке соков производится с учетом трех обстоятельств. 1. Активности фермента. для получения желаемого действия при производстве фруктовых соков необходимо подобрать правильную концентрацию, температуру и продолжительность обработки. 2. Необходимости деградации пектина. Качество продукции сильно зависит от типа пектина и свойств конкретного фермента. 3. Механизмов осветления. Этот процесс состоит из трех последовательных стадий. Понимание их особенностей исключительно важно при производстве соков: это стадии дестабилизации, коагуляции и осаждения. При производстве соков из фруктов большую роль играют пектины. Если их слишком много, то соки получаются излишне вязкими и мутными. Контролируя содержание пектинов, удается существенно повысить выход сока и его качество. Пектиновые вещества, или пектины, представляют собой гетерополисахаридьт, производные галактуроновой кислоты. Они являются. субстратами для ряда ферментов: пектинлиаз, пектатлиаз, полигалактуронидаз или пектинэстераз. действие их заключается в деполимеризации путем расщепления глюкозидных связей лектиноэстеразы атакуют этерифицированные карбоксильные группы.
| <== предыдущая страница | | | следующая страница ==> |
| Введение 10 страница | | | Генетически-модифицированные продукты. Гигиеническая систематика пищевых добавок |
Дата добавления: 2014-02-27; просмотров: 2621; Нарушение авторских прав

Мы поможем в написании ваших работ!