
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Потенциал его определяемся соотношением
КАЛОМЕЛЬНЫЙ ЭЛЕКТРОД
Если металлический электрод покрыть слоем малорастворимой соли, этого металла и опустить в раствор хорошо растворимой соли, содержащей тот же анион, то такой электрод работает обратимо относительно этого аниона. К таким электродам принадлежит каломельный электрод.

В нем паста из ртути и каломели (Hg2Cl2 ) помещается в раствор KCl (обычно 1н или насыщенный).
Процесс отвечает записи
Cl- (aCl-) ½Hg2Cl2, Hg.
На электроде протекает реакция
2Hg + 2Cl- = Hg2Cl2 + 2e.
j = j0кал – lnaCl-.
Он является, таким образом, хлорным электродом, в котором ионы хлора поступают не от газообразного Cl2а от твердого хлорида ртути. Потенциал этого электрода по нормальному водородному электроду при 25°С при 1н растворе=+0,2819 в.
Ввиду вредности работы с ртутью в последние годы шире применяют аналогичный каломельному - хлорсеребряный электрод.
7.3.8 ИЗМЕРЕНИЕ ЭДС. НОРМАЛЬНЫЙ ЭЛЕМЕНТ
При работе гальванического элемента его ЭДС не сохраняет строго постоянного значения вследствие изменения концентрации растворов и других причин. Поэтому точные измерения ЭДС должны производиться при минимальном прохождении тока. Этому отвечает компенсационный метод измерения ЭДС, дающий возможность определить ЭДС элемента путем измерения разности потенциалов в условиях обратимой работы элемента.
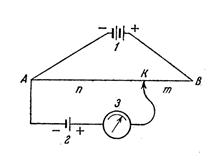
Источник тока 1 с известной ЭДС, например, аккуммулятор, замкнут через проволоку АВ. Проволока должна обладать одинаковым сопротивлением по всей длине. При этом условии падение напряжения на всем протяжении ее от А до В пропорционально длине проволоки. Проволока натянута вдоль шкалы. В боковую цепь включены последовательно измеряемый элемент 2и чувствительный гальванометр 3. Перемещая подвижный контакт К, можно подобрать такое расположение его, при котором ЭДС элемента будет точно компенсироваться и в боковой цепи ток проходить не будет. Это означает, что падение потенциала вдоль проволоки на участке АК будет точно равно ЭДС измеряемого элемента Е. Зная длину n этого участка проволоки АК, длину m остальной части КБ и ЭДС источника 1,равную Е1, можно определить
Е2 = Е1 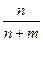 .
.
При измерениях ЭДС часто возникает необходимость иметь вспомогательный элемент с хорошо известной и устойчивой ЭДС .Для этой цели применяют так называемый нормальный элемент (элемент Вестона).
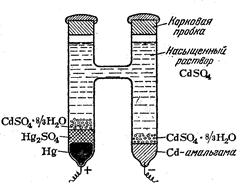
В нем отрицательный электрод представляет собой амальгаму кадмия, помещенную в раствор сульфата кадмия, насыщенный относительно кристаллогидрата CdSO4 ×H2O и находящийся в постоянном соприкосновении с ним, положительный электрод представляет пасту из ртути и Hg2SO4 , помещенную в тот же раствор, насыщенный относительно CdSO4 ×H2O. Для лучшего контакта с вводом под пасту помещается некоторое количество ртути. Положительный электрод в этом элементе подобен каломельному, но работает обратимо в отношении ионов SO42-. Отрицательный электрод принадлежит к амальгамным электродам.
При работе этого элемента протекает реакция
Cd + Hg2SO4 + H2O = CdSO4× H2O + 2Hg.
При кратковременном замыкании, например, в случае применения элемента для компенсационных целей, он работает вполне обратимо и устойчиво. Последнее обусловлено тем, что оба электрода находятся в насыщенном растворе.
При 20°C его ЭДС Е = 1,01830 в.
| <== предыдущая страница | | | следующая страница ==> |
| Окислительно-восстановительные электроды | | | К цепям второго рода относятся цепи с газовыми или амальгамными электродами |
Дата добавления: 2014-03-11; просмотров: 343; Нарушение авторских прав

Мы поможем в написании ваших работ!