
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Классификация окислительно-восстановительных рекаций
Обычно выделяют три типа окислительно-восстановительных реакций: межмолекулярные, внутримолекулярные и реакции диспропорционирования.
8.1. Реакции межмолекулярного окисления-восстановления:
окислитель и восстановитель входят в состав разных веществ. Примером такой реакции служит взаимодействие между цинком и дихроматом калия, рассмотренное выше.
В реакциях межмолекулярного окисления-восстановления не обязательно, чтобы взаимодействовали атомы разных элементов; эти реакции могут происходить между атомами одного и того же элемента, но при условии, что они имеют различные степени окисления:
: 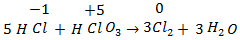
Иногда могут одновременно окисляться или восстанавливаться сразу несколько элементов:
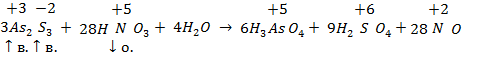
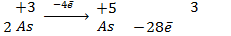
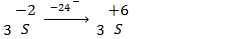
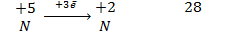
8.2. Реакции внутримолекулярного окисления-восстановления:
окислитель и восстановитель входят в состав одного и того же вещества.
Опыт «Химический вулкан»
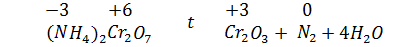
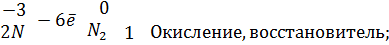
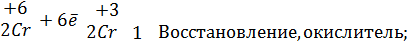
8.3. Реакции самоокисления-самовосстановления (диспропорционирования:один и тот же элемент выполняет функции и окислителя, и восстановителя.
Опыт «Выведение пятен от иодной настойки»
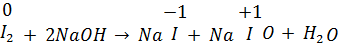
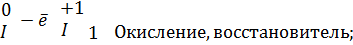
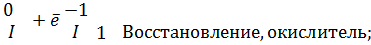
Мы видим, что одни атомы иода повышают свою степень окисления и проявляют свойства восстановителей, а другие атомы иода понижают степень окисления и проявляют свойства окислителей; таким образом, степень окисления иода – исходного вещества – является промежуточной.
| <== предыдущая страница | | | следующая страница ==> |
| | | Влияние среды на направление ОВР |
Дата добавления: 2014-05-02; просмотров: 379; Нарушение авторских прав

Мы поможем в написании ваших работ!